Publié sur :
Document Nicole Delépine - 2009
Voir la version PDF de cette publication :

Tumeurs Osseuses bénignes du genou
G. Delepine,
Nicole Delepine
Tumeurs Osseuses bénignes du genou
La pathologie tumorale primitive du genou est protéiforme
A coté des tumeurs osseuses bénignes et des dystrophies pseudotumorales qui constituent cette présentation, il faut insister sur la prise en charge sans faute qu'imposent les sarcomes osseux.
Sur la fréquence des tumeurs bénignes des parties molles et l'existence des sarcomes des parties molles avant de schématiser la conduite initiale rigoureuse indispensable pour faire bénéficier le malade des progrès thérapeutiques récents dans les sarcomes.
Tumeurs cartilagineuses
Exostoses ostéogéniques
Chondromes
Chondroblastomes
Fibromes chondromyxoïde
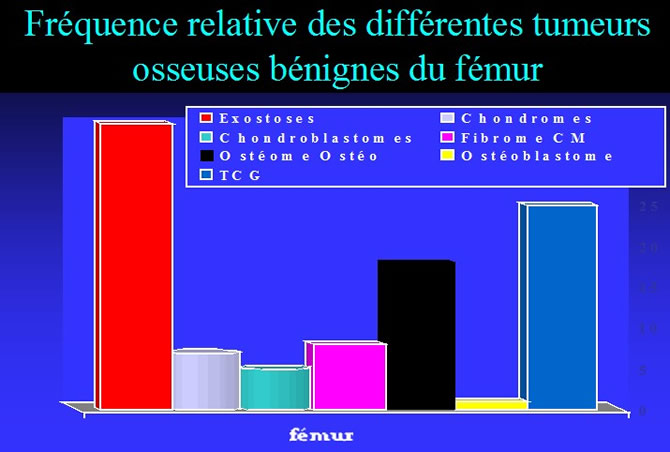
Les plus fréquentes des Tumeurs Osseuses Bénignes : 40%
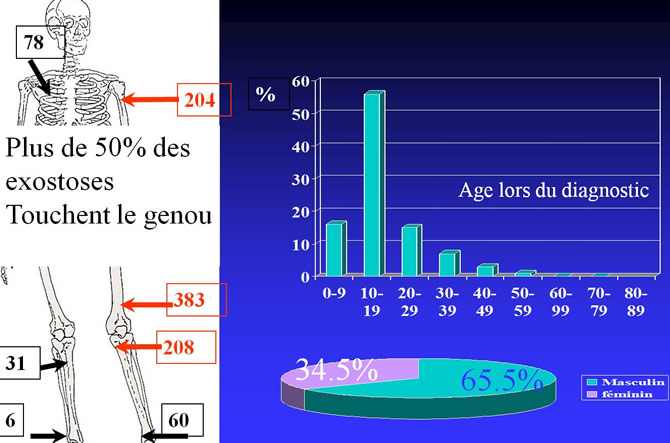
 Répartition par sexe, age et topographies de 1177 Exostoses
Répartition par sexe, age et topographies de 1177 Exostoses
Plus de 50% des exostoses touchent le genou.
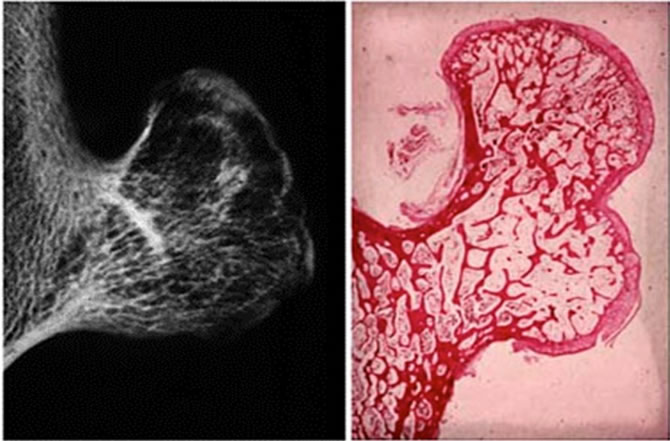
 L'exostose ostéogénique est un cartilage de croissance mal orientée (latéralement)
L'exostose ostéogénique est un cartilage de croissance mal orientée (latéralement)
 La coiffe cartilagineuse est la partie active de l'exostose, celle qui crée le socle osseux
La coiffe cartilagineuse est la partie active de l'exostose, celle qui crée le socle osseux
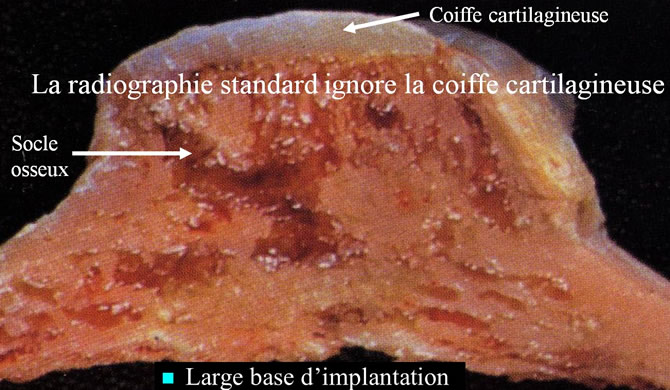 La radiographie ignore la coiffe cartilagineuse
La radiographie ignore la coiffe cartilagineuse
La détermination de l'épaisseur de la coiffe cartilagineuse d'une exostose permet d'évaluer son potentiel évolutif et son risque de dégénérescence.
Comme le cartilage est radio transparent cette mesure ne peut être réalisée qu'au scanner ou à l'IRM.
 La mesure de l'épaisseur du cartilage est indispensable par scanner ou IRM
La mesure de l'épaisseur du cartilage est indispensable par scanner ou IRM
En IRM le cartilage périphérique, gorgé d'eau se distingue très facilement du socle osseux par son signal hydrique.
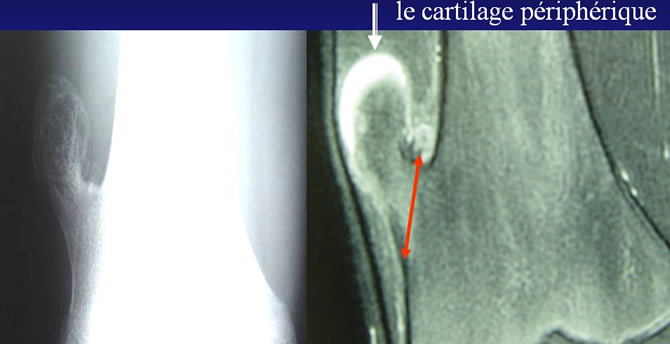 Les exostoses peuvent être solitaires
Les exostoses peuvent être solitaires
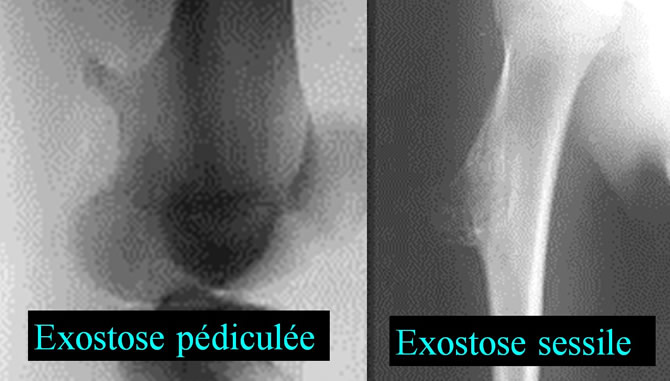 Bifide
Bifide
Longue exostose bifide pédiculée à partir du péroné.
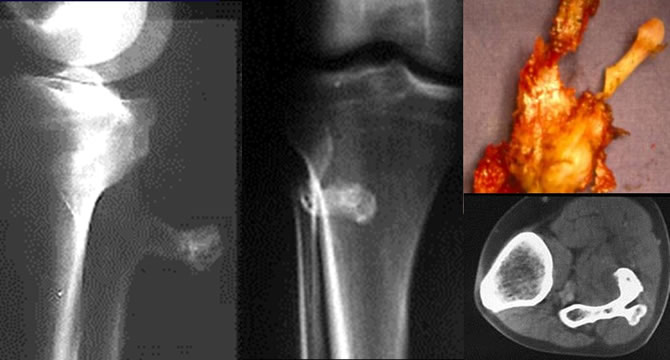 Ou exprimer une maladie exostosante
Ou exprimer une maladie exostosante
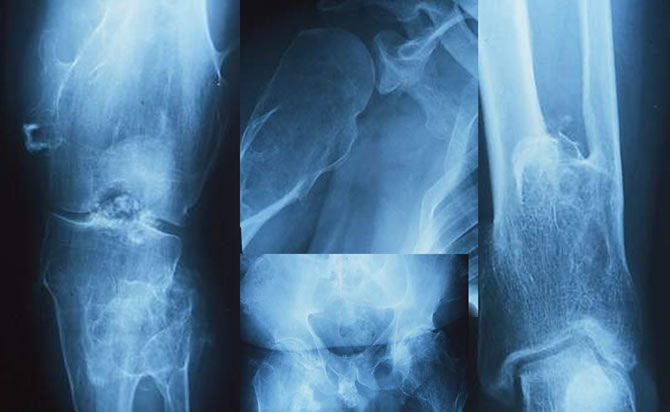 Il n'y a pas de parallélisme entre la taille de l'exostose et ses signes cliniques
Il n'y a pas de parallélisme entre la taille de l'exostose et ses signes cliniques
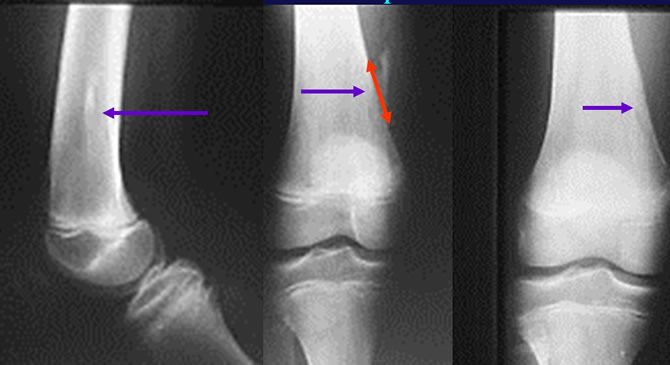
Petite exostose peu visible mais très symptomatique :
Jeune homme de 13 ans venu consulter pour des douleurs de la face antérieure du genou avec sensations de blocages transitoires lors de certains mouvements de flexion.
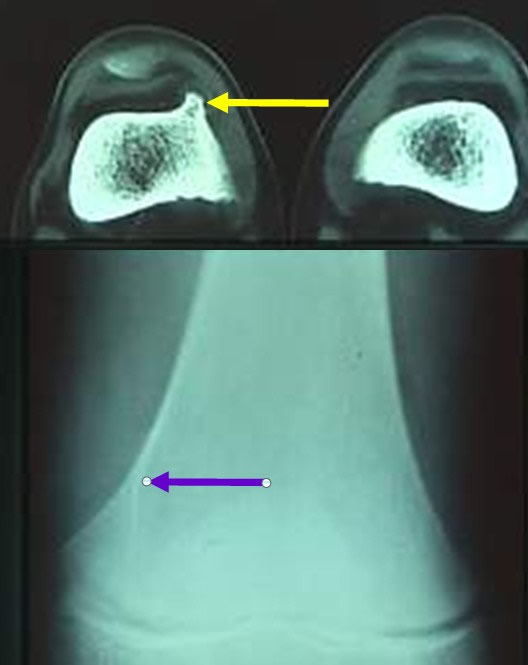 Évolution spontanée
Évolution spontanée
Régression spontanée lors de la croissance d'une exostose sessile de la métaphyse fémorale inférieure.
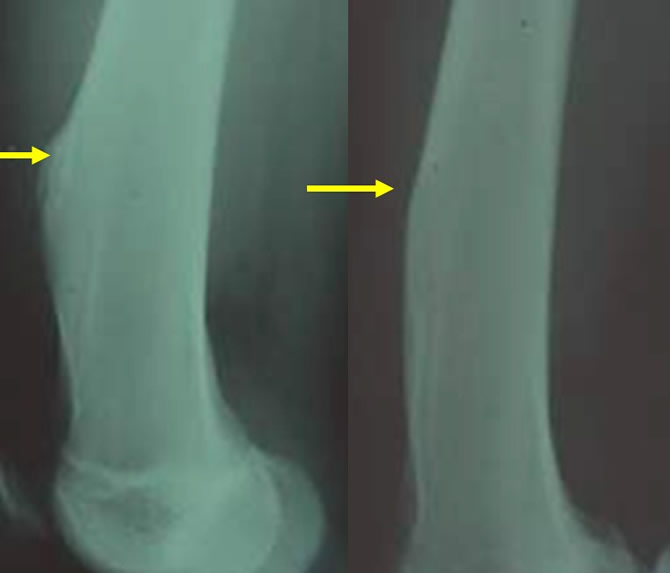 Les exostoses peuvent comprimer les artères
Les exostoses peuvent comprimer les artères
La compression artérielle peut entraîner de pseudo anévrysme et doit être levée.
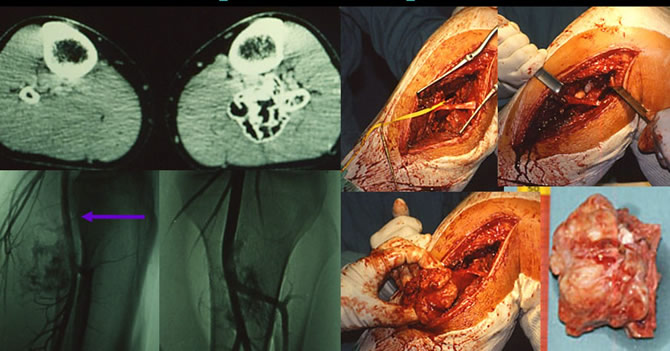 Les exostoses peuvent comprimer les veines
Les exostoses peuvent comprimer les veines
Exostose révélée par une grosse jambe d'apparition lente. La menace de thrombose veineuse et de ses complications emboliques justifient une éxérèse chirurgicale.
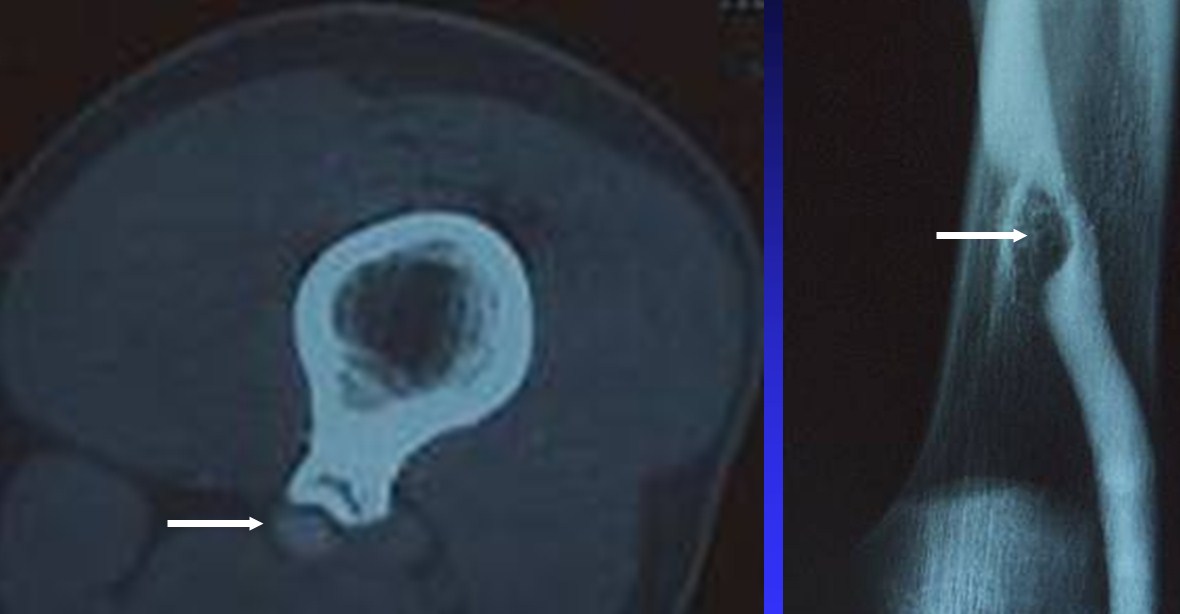 Traitement chirurgical d'une exostose pédiculée : sectionner le pédicule
Traitement chirurgical d'une exostose pédiculée : sectionner le pédicule
La guérison est obtenue après une résection qui n'a pas fragilisé l'os.
 En cas d'exostose sessile le remodelage de l'os est plus lent
En cas d'exostose sessile le remodelage de l'os est plus lent
 Traitement des exostoses de l'enfant
Traitement des exostoses de l'enfant
N'opérer que les exostoses symptomatiques mal tolérées.
N'opérer qu'en fin de croissance (si possible).
Lorsqu'enlever toute l'exostose risque de léser le cartilage de croissance il est prudent de n'enlever que la partie gênante.
 Dégénérescence des exostoses
Dégénérescence des exostoses
Bénignité habituelle.
Risque de dégénérescence maligne : 1%
Se méfier :
- des exostoses de l'adulte
- centrale ou proximale
- devenues symptomatiques
- rapidement évolutives
- avec modifications radiologiques (lacunes à la base et calcifications à distance)
- quand la coiffe cartilagineuse a plus de 5 mm.
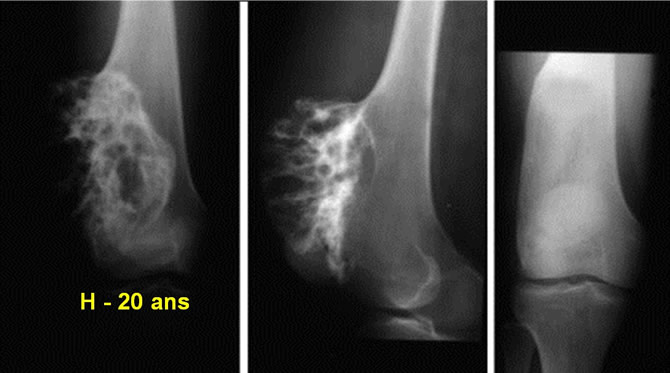
Dégénérescence d'une exostose fémorale
Malade de 42 ans, exostose ancienne peu symptomatique jusqu'il y a 2 mois.
Depuis douleurs et tuméfaction croissante.
Exérèse large d'emblée confirmant la dégénérescence.
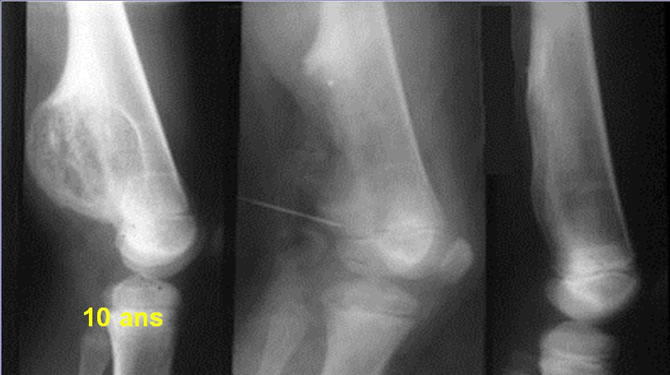
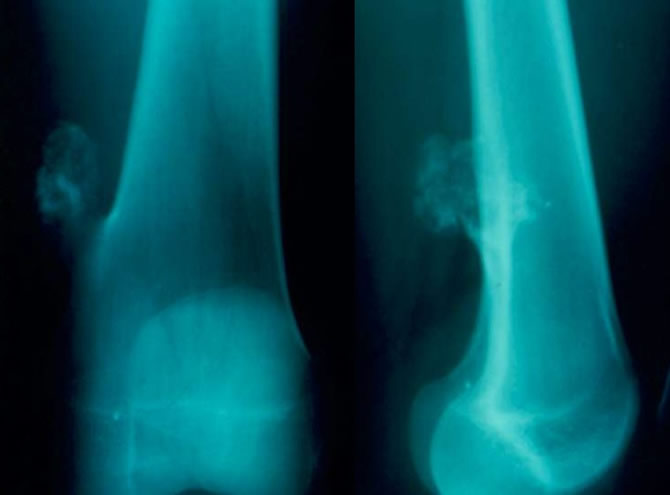 Dégénérescence d'une exostose tibiale
Dégénérescence d'une exostose tibiale
Malade de 26 ans ayant remarqué depuis 4 mois une tuméfaction peu douloureuse progressivement croissante du genou.
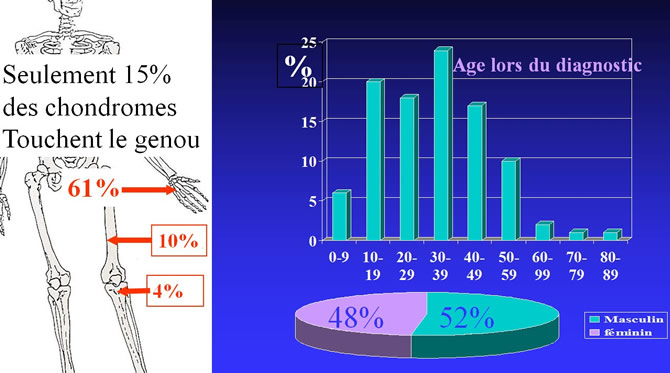
 Répartition par sexe, age et topographies de 481 chondromes
Répartition par sexe, age et topographies de 481 chondromes
Seulement 15% des chondromes touchent le genou.
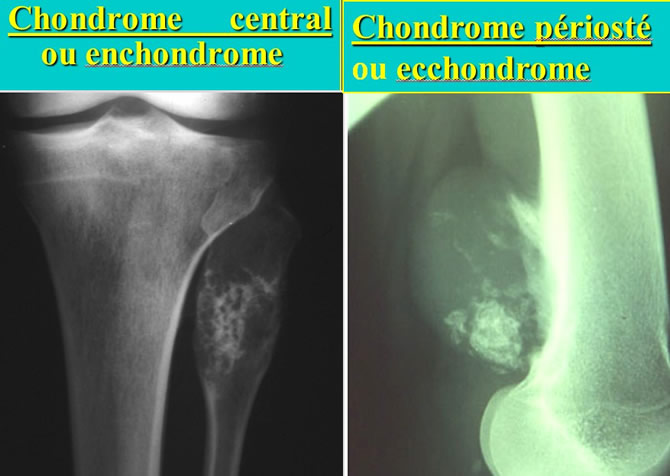
 Formes topographiques des chondromes
Formes topographiques des chondromes
Centraux : 85%, périostés : 15%.
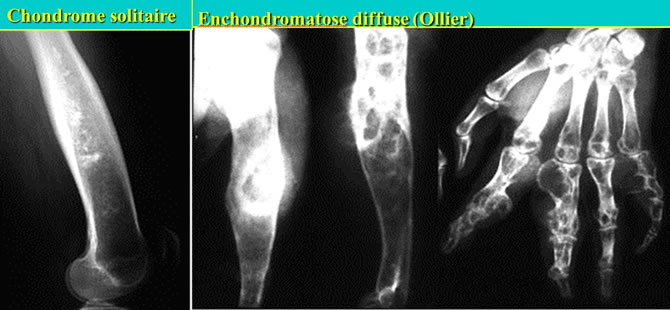
 Unique ou multiple ?
Unique ou multiple ?
Métaphyses ++
Asymétrie des lésions (unilatéralité dans 50%)
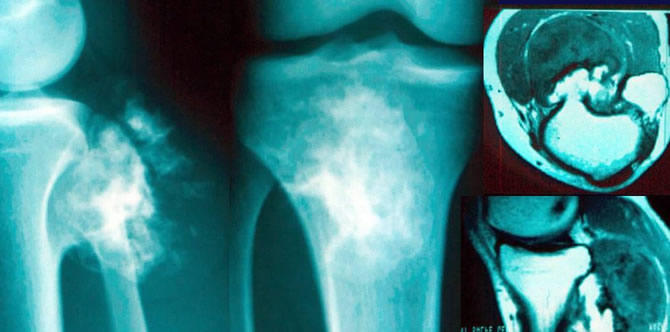
 Radiologie des chondromes
Radiologie des chondromes
Métaphyse, métaphyso-diaphyse.
Géode claire, homogène, arrondie, nette.
Trabéculations fines ou petites opacités punctiformes.
Les calcifications floconneuses signent la nature cartilagineuse de la tumeur.
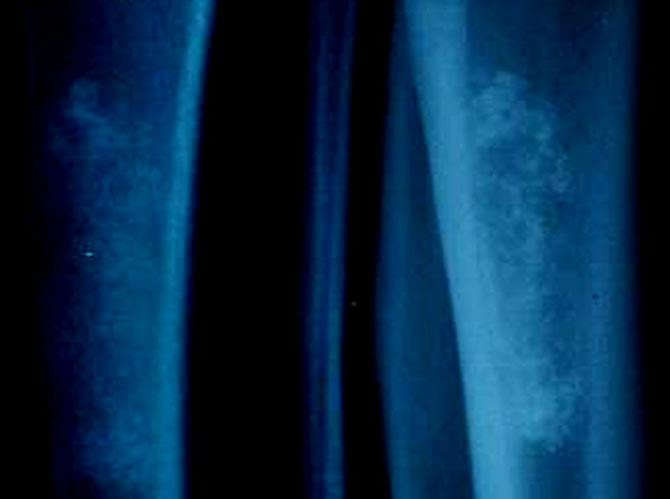
 Enchondromes fémoraux typiques
Enchondromes fémoraux typiques
Images floconneuses à l'intérieur de la cavité médullaire.
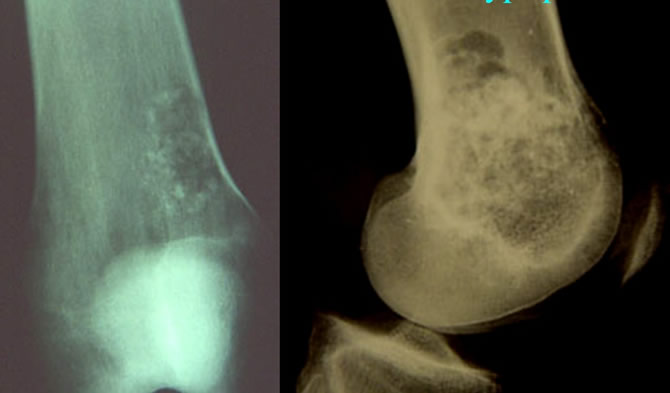 Enchondrome tibial typique
Enchondrome tibial typique
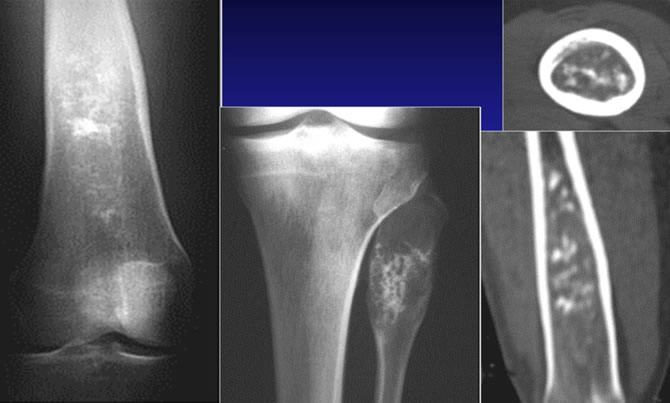
 Chondrome fémoral faiblement calcifié
Chondrome fémoral faiblement calcifié
Les calcifications débutantes sont mieux mises en évidence sur le scanner ou l'IRM.
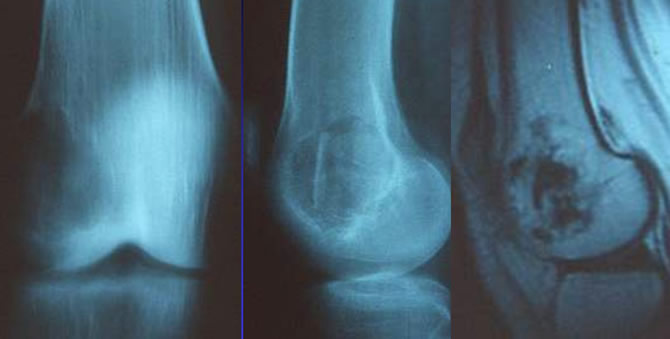 Chondrome jeune, non calcifié
Chondrome jeune, non calcifié
les calcifications apparaissent tardivement sur des chondromes vieillis, en partie nécrosés, mal vascularisés.
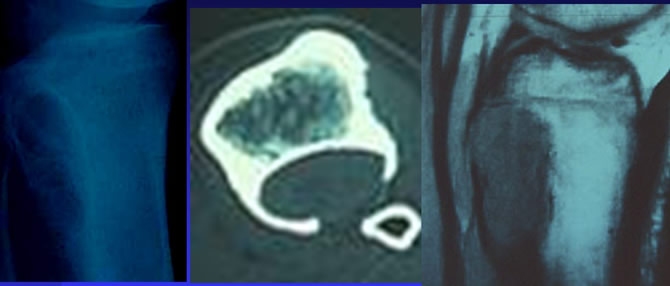 Évolution des chondromes
Évolution des chondromes
Récidive rare, après traitement chirurgical correct qu'il s'agisse de curettage comblement (enchondrome) ou d'une résection.
Fracture pathologique assez fréquement révélatrice à la main.
Inégalités et déviations des membres s'observe surtout dans la maladie d'Ollier
Transformations malignes en chondrosarcomes :
- rares pour les chondromes solitaires.
- 20% des cas d'enchondromatose.
Traitement chirurgical d'un enchondrome
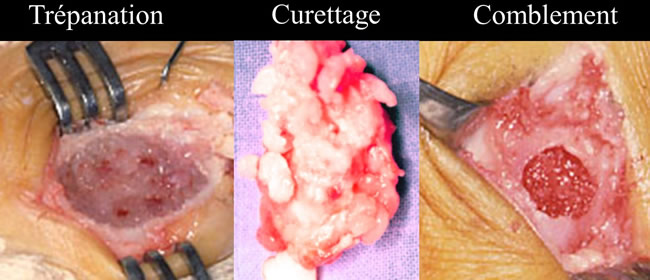 Résection d'un chondrome de la tête du péroné
Résection d'un chondrome de la tête du péroné
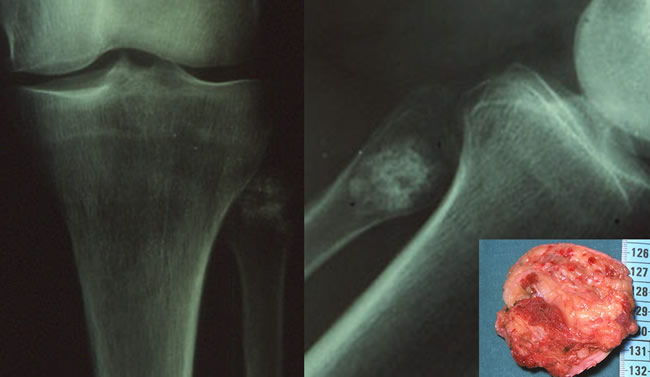 Transformations malignes en chondrosarcomes :
Transformations malignes en chondrosarcomes :
Rares pour les chondromes solitaires 20% des cas d'enchondromatose.
Douleurs du genou chez une femme de 45 ans souffrant d'enchondromatose multiple. La scintigraphie osseuse hyperfixante et la radiographie de profil doivent inquiéter.
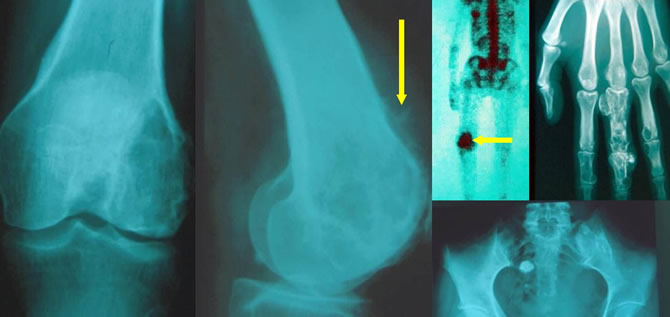 Douleurs du genou chez une femme de 45 ans souffrant d'enchondromatose multiple (suite)
Douleurs du genou chez une femme de 45 ans souffrant d'enchondromatose multiple (suite)
Biopsie chirurgicale confirmant le chondrosarcome dédifférencié.
Bilan révélant des métastases pulmonaires.
Évolution défavorable.
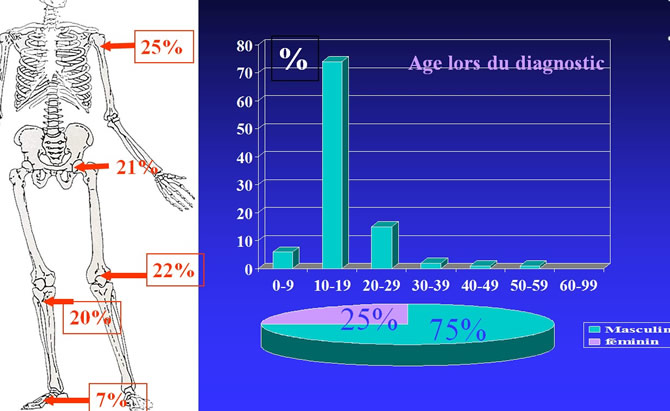
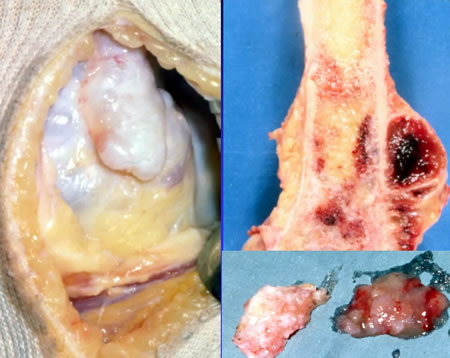 Répartition par sexe, topographies et age de 247 chondroblastomes
Répartition par sexe, topographies et age de 247 chondroblastomes
 Chondroblastome des épines tibiales
Chondroblastome des épines tibiales
Lyse osseuse épiphysaire limitée : Géode arrondie ou ovalaire.
Cerclée par un liseré de condensation,
Contenu homogène (cloisons rares),
Os parfois soufflé.
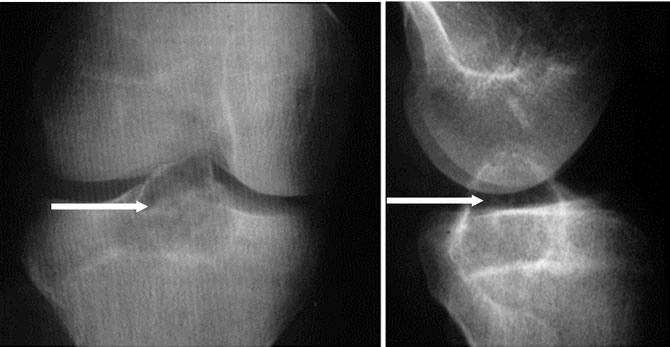 Chondroblastome fémoral
Chondroblastome fémoral
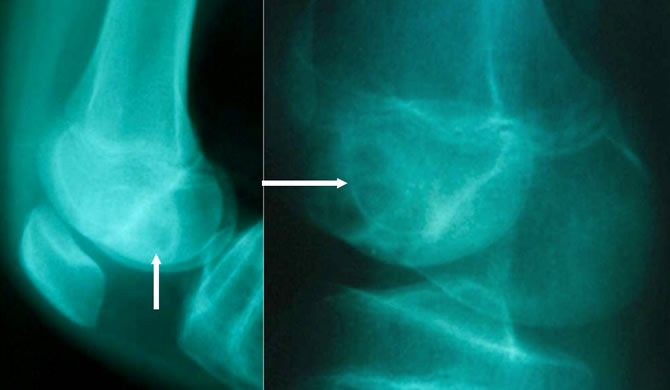 Chondroblastome tibial historique
Chondroblastome tibial historique
Malade de 19 ans souffrant depuis 3 ans de son genou.
Flessum iréductible.
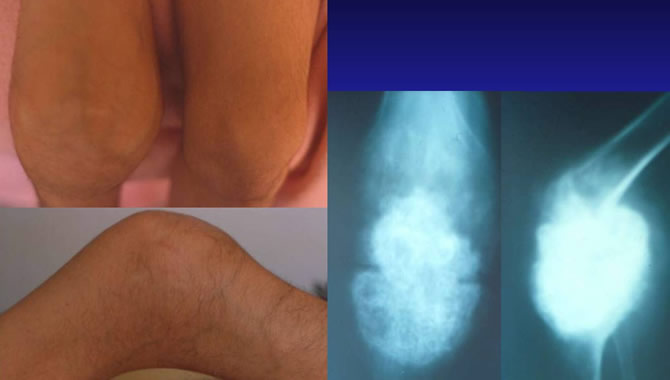 Répartition par sexe, topographies et age de 73 Firomes chondromyxoides
Répartition par sexe, topographies et age de 73 Firomes chondromyxoides
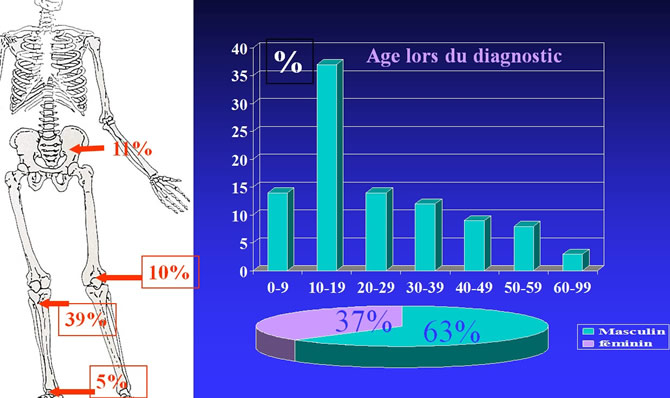 Radiologie des fibromes chondromyxoïdes
Radiologie des fibromes chondromyxoïdes
Lacune métaphysaire excentrée, Limites nettes avec ostéosclérose réactionnelle, rares calcifications intra-tumorales.
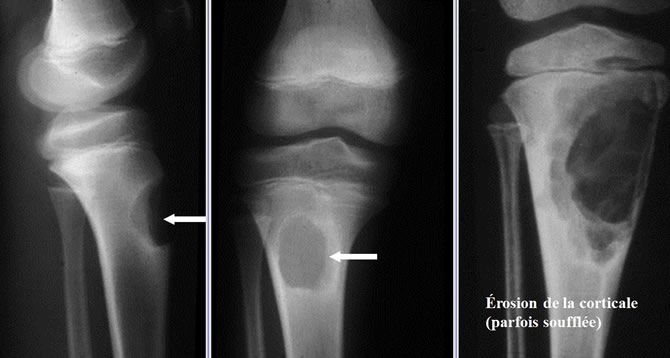 Fibrome chondromyxoide du condyle interne chez un adolescent de 17 ans
Fibrome chondromyxoide du condyle interne chez un adolescent de 17 ans
Douleurs sans anomalies radiologiques majeures du fémur.
Sur l'IRM lacune en hypersignal de type cartilagineux.
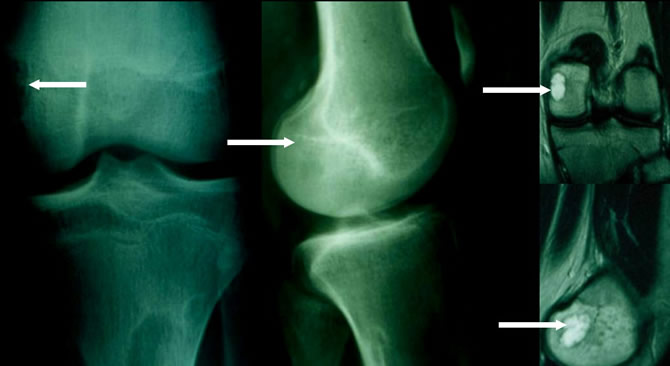 Traitement des fibromes chondromyxoïdes
Traitement des fibromes chondromyxoïdes
Chirurgie conservatrice. Excision complète ou curetage + comblement.
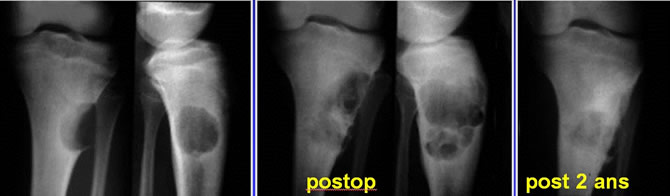 Fibrome chondromyxoide du fémur inférieur chez un enfant de 10 ans
Fibrome chondromyxoide du fémur inférieur chez un enfant de 10 ans
Février 1992. Vaste lacune ovalaire bien limitée rompant la corticale postérieure sans calcification intratumorale.
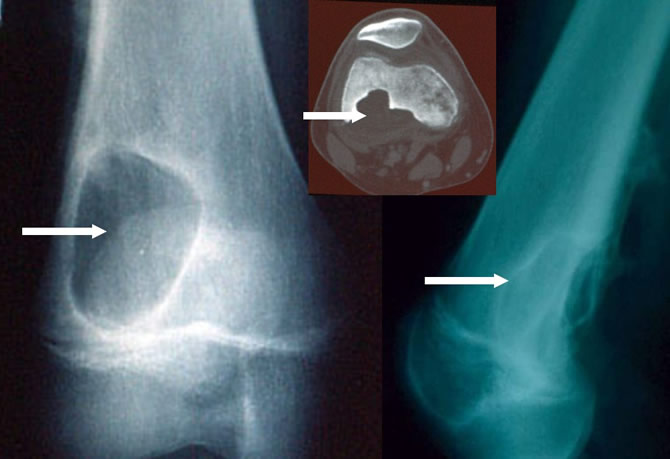 8 ans plus tard
8 ans plus tard
Après 2 récidives et 3 curettages comblements osseux stabilisation des lésions osseuses mais réapparition d'une reprise évolutive dans ls parties molles postérieures.
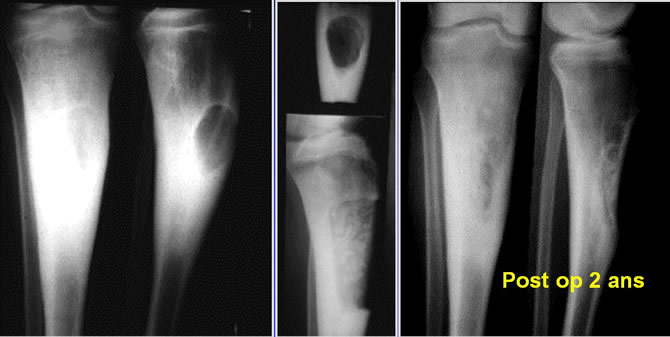
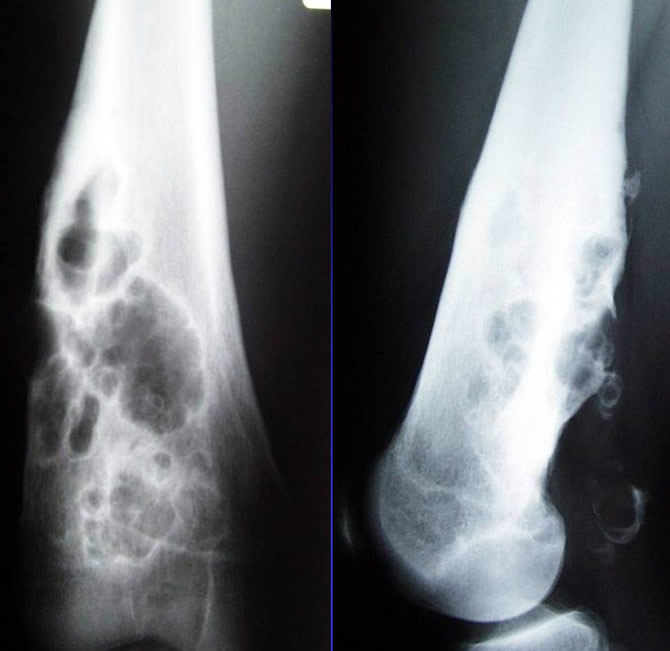 Traitement des fibromes chondromyxoïdes H - 15 ans
Traitement des fibromes chondromyxoïdes H - 15 ans
Excision + comblement.
 Répartition par topographies de 1444 Tumeurs à cellules géantes
Répartition par topographies de 1444 Tumeurs à cellules géantes
Tumeur épiphyso-métaphysaire.
Des os longs des membres.
50% des cas touchent le genou.
10% l'extrémité inférieure du radius.
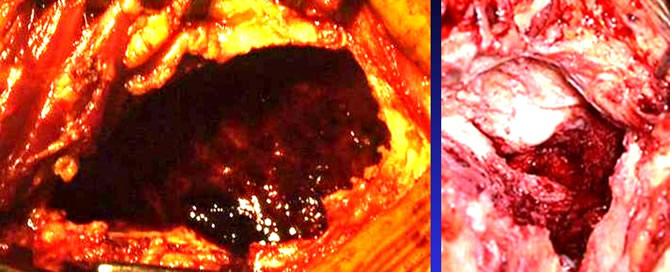
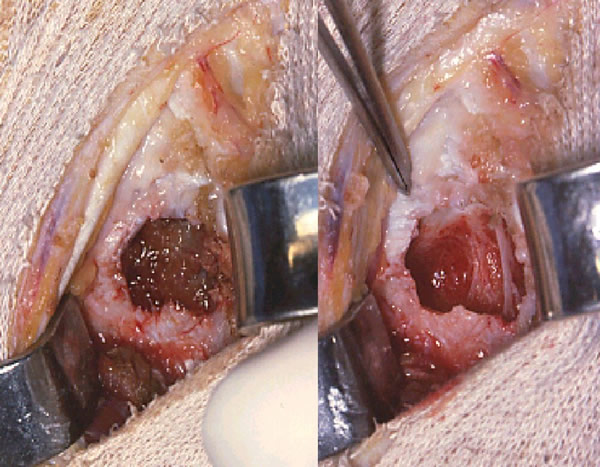
 Aspect macroscopique
Aspect macroscopique
Tumeur rougeâtre ou brune, avec quelques zones blanchâtres.
Enclose dans une cavité osseuse. Respecte le cartilage articulaire.
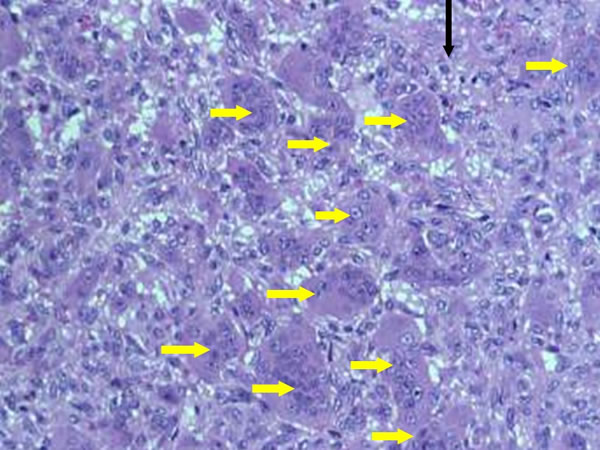
 Tumeurs à cellules géantes : Aspect microscopique
Tumeurs à cellules géantes : Aspect microscopique
1°) Fond homogène de cellules rondes ou ovalaires, a noyau arrondi et chromatine fine.
2°) cellules géantes plurinucléées (de 30 à 100 noyaux) irrégulièrement réparties.
3°) mitoses rares.
4°)Présence de phosphatases acides.
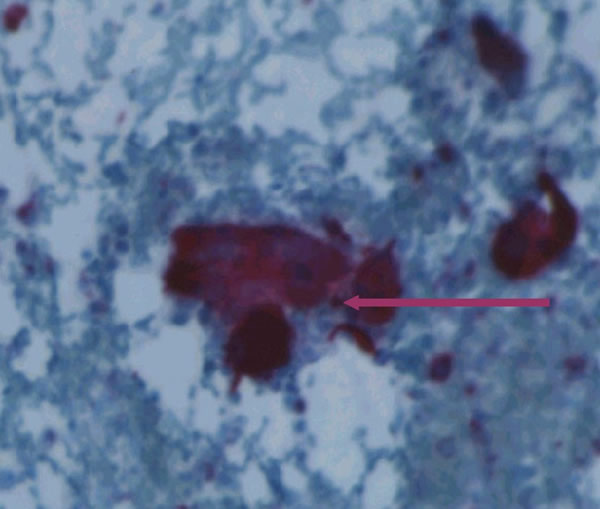
 Tumeurs à cellules géantes : Aspect microscopique
Tumeurs à cellules géantes : Aspect microscopique
Les réactions histochimiques montrent la présence de phosphatases acides dans le cytoplasme des cellules géantes et de quelques cellules mononucléées.
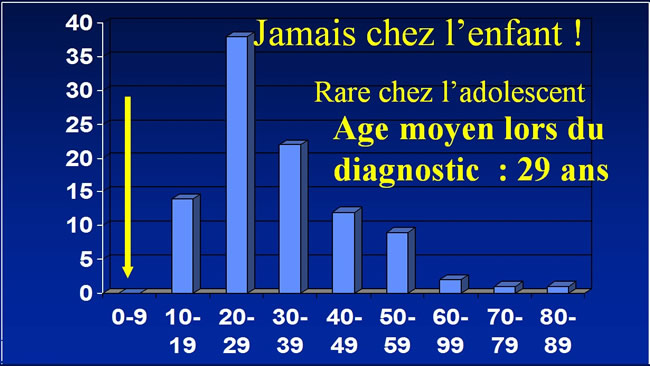
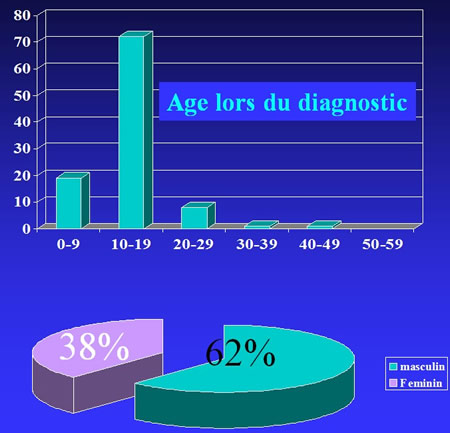
 Age des malades lors du diagnostic de Tumeurs à cellules géantes
Age des malades lors du diagnostic de Tumeurs à cellules géantes
1444 cas extraits de 10 séries. 80 % des cas touchent des Adultes jeunes entre 20et 40 ans.
 Aspect radiologique typique
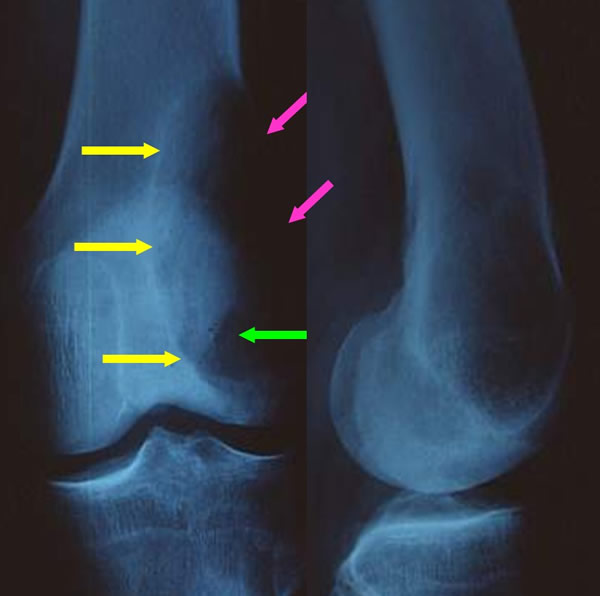
Aspect radiologique typique
Lacune épiphyso métaphysaire lytique pure
Ovalaire ou arrondie
Discrète soufflure de l'os
Parfois trabéculée
Limitée par un fin liseré condensé
 Aspect tomodensitométrique typique
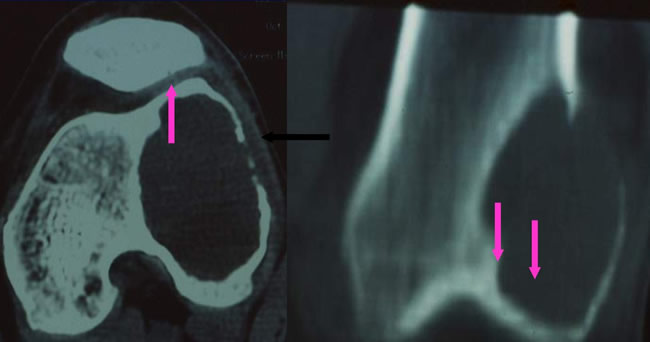
Aspect tomodensitométrique typique
Persistance d'une corticale continue, parfois en pointillée
Respect du cartilage articulaire
Pas d'envahissement des parties molles
 Classification radiologique (Meary)
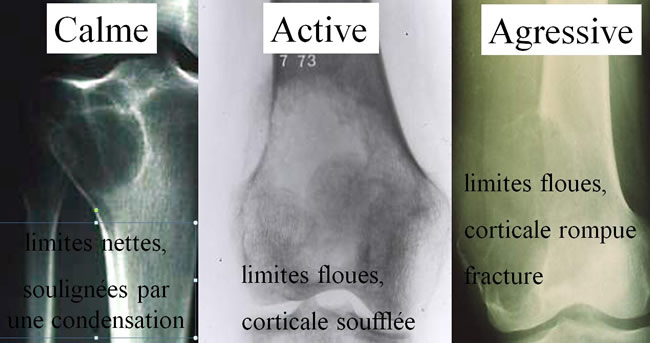
Classification radiologique (Meary)
Aucune corrélation notable avec l'aspect histologique ni avec l'évolution ultérieure (risque de récidive...)
 Tumeurs à cellules géantes calmes
Tumeurs à cellules géantes calmes
Limites nettes, condensées, Cloisons.
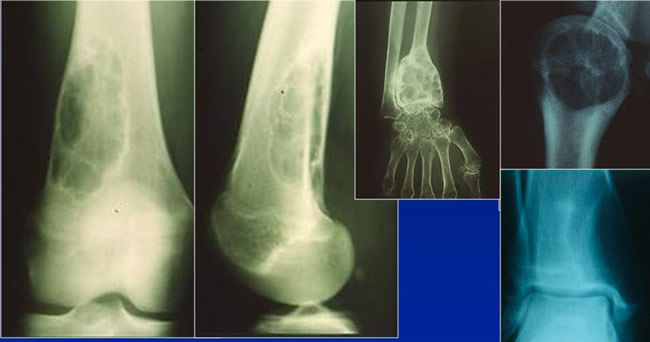 Tumeur agressive : rupture corticale et envahissement des parties molles
Tumeur agressive : rupture corticale et envahissement des parties molles
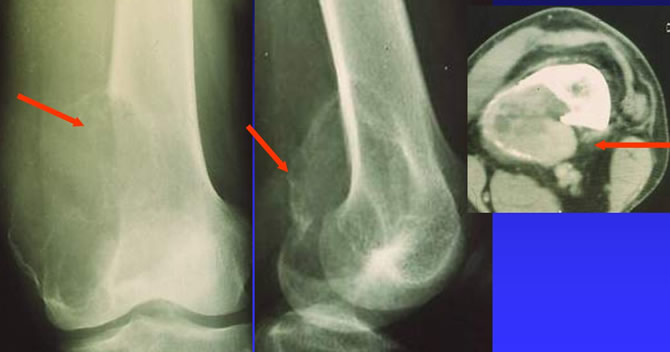 Tumeur à cellules géantes agressive révélée par une fracture déplacée chez une femme de 48 ans
Tumeur à cellules géantes agressive révélée par une fracture déplacée chez une femme de 48 ans
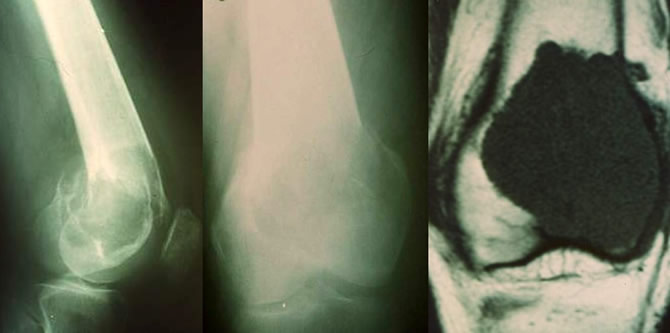 La tumeur à cellules géantes bénigne peut envahir les parties molles
La tumeur à cellules géantes bénigne peut envahir les parties molles
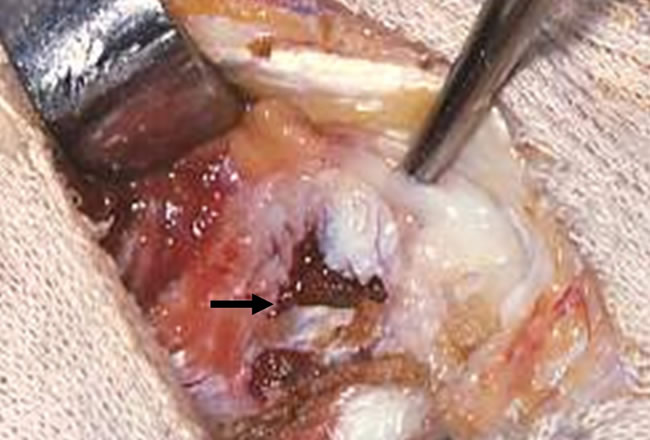 Techniques chirurgicales possibles
Techniques chirurgicales possibles
- Curettage,
- Complété ou non d'adjuvants (Cryothérapie ou Phénol),
- Suivi de comblement spongieux ou de comblement ciment,
- Résection,
- Suivi de reconstruction épiphysaire, ou d'arthrodèse, ou de prothèse massive.
Le Curettage simple est peu efficace
Plus de 60% de récidive dans la série de Bonfiglio.
Le comblement de la cavité est indispensable.
Le curettage comblement osseux est suivi de nombreuses récidives locales !
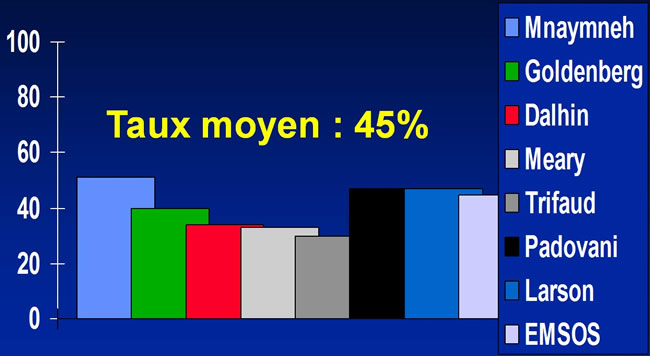 Date des récidives après curettage comblement osseux
Date des récidives après curettage comblement osseux
 Exemple d'échec après comblement spongieux
Exemple d'échec après comblement spongieux
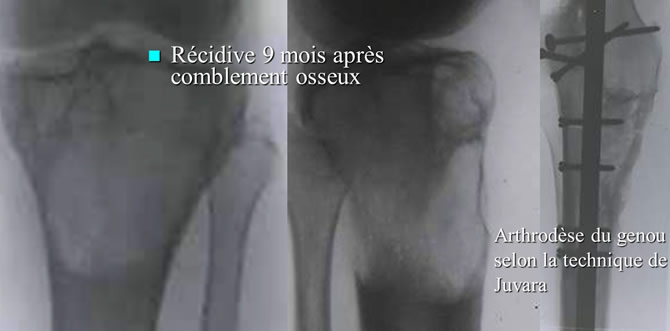
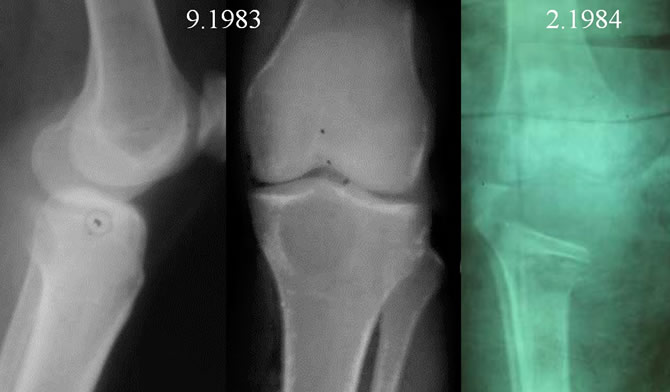 Risque des Tumeurs à cellules Géantes : Perte de l'articulation
Risque des Tumeurs à cellules Géantes : Perte de l'articulation
Récidive 9 mois après comblement osseux.
Arthrodèse du genou selon la technique de Juvara.
 Facteurs de réussite
Facteurs de réussite
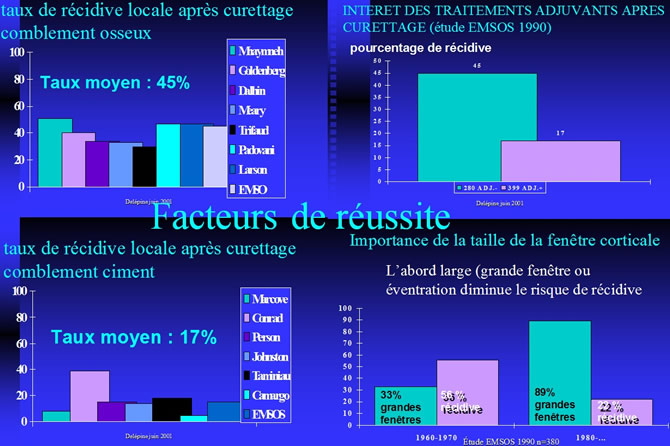 Éventration comblement ciment
Éventration comblement ciment
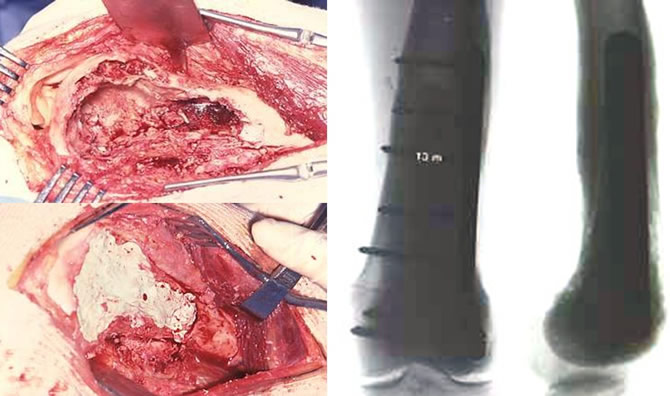 Traitement par éventration curettage comblement ciment d'une Tumeur à cellules géantes agressive
Traitement par éventration curettage comblement ciment d'une Tumeur à cellules géantes agressive
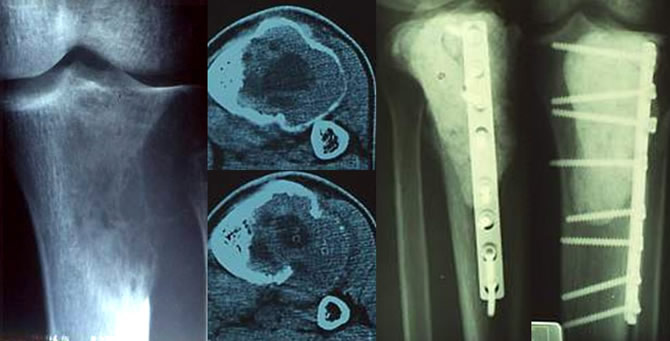 Éventration Comblement Ciment d'une TCG au contact du cartilage articulaire
Éventration Comblement Ciment d'une TCG au contact du cartilage articulaire
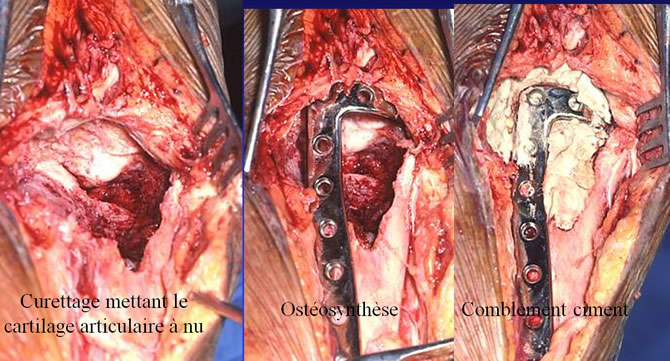 La reconstruction au ciment est possible même en cas de fracture du cartilage articulaire
La reconstruction au ciment est possible même en cas de fracture du cartilage articulaire
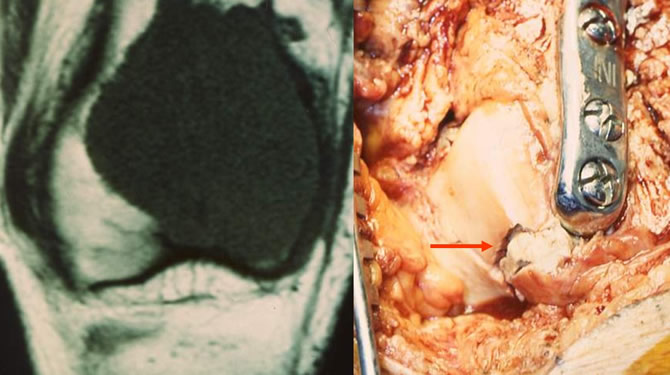 Résultat radiologique 15 ans après traitement d'une tumeur fracturée
Résultat radiologique 15 ans après traitement d'une tumeur fracturée
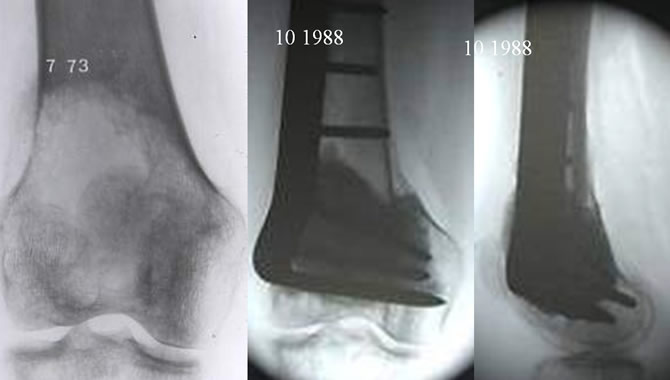 Le comblement ciment n'empêche pas la consolidation radiologique
Le comblement ciment n'empêche pas la consolidation radiologique
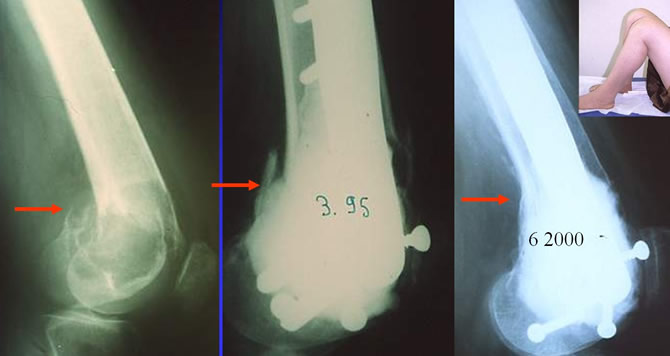 Après comblement ciment la fonction est quasi normale
Après comblement ciment la fonction est quasi normale
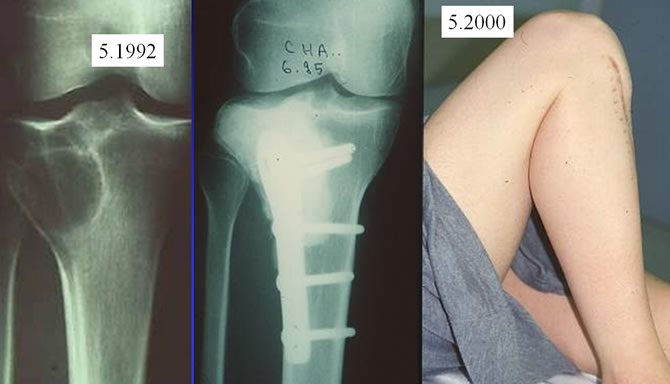 Fonction après comblement ciment
Fonction après comblement ciment
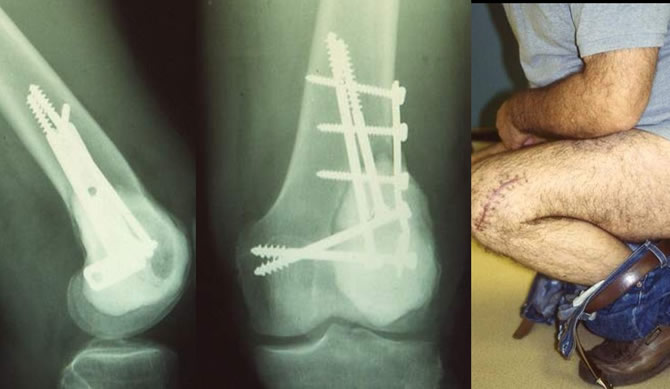 Résultat après traitement d'une tumeur fracturée
Résultat après traitement d'une tumeur fracturée
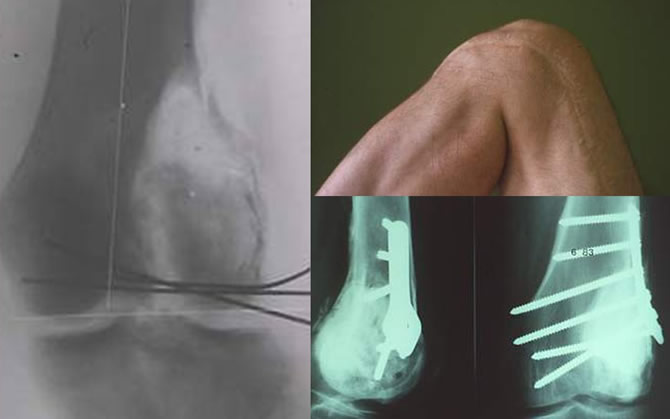 Récidive sur ciment
Récidive sur ciment
La surveillance radiologique est facilitée par le comblement au ciment :
Tout liseré de plus de 2 millimètres apparu autour du ciment représente un signe formel de récidive.
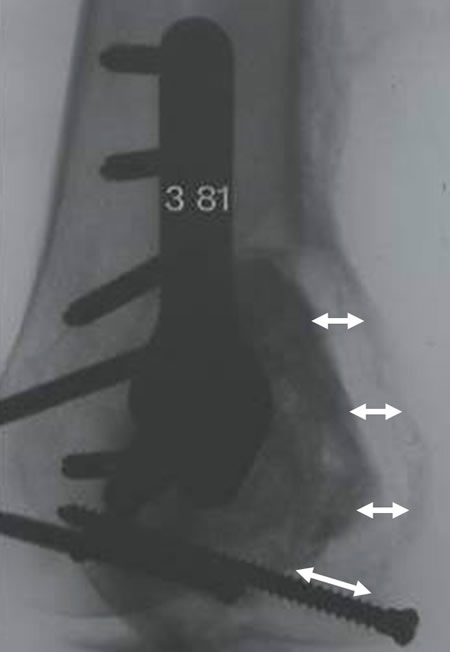 Avantages du ciment :
Avantages du ciment :
1°) absence de prélèvement osseux.
2°) usage immédiat et libre du membre opéré.
3°) surveillance radiologique postopératoire facile.
4°) excellent taux de sauvegarde articulaire à long terme même en cas de tumeur du radius, agressive, récidivée...
Tumeurs à cellules géantes malignes
Après irradiation une tumeur à cellules géantes bénigne peut se transformer en tumeur maligne (25% des cas d'après Dalhin).
il s'agit le plus souvent de sarcome riche en cellules géantes (Histiocytofibrome malin) mais il peut aussi s'agir d'ostéosarcome, de fibrosarcome, de sarcome anaplasique, telangiectasique...
Certaines tumeurs riches en cellules géantes sont malignes d'emblée. Elles se classent parmi les histiocytome fibreux malins.
Transformation maligne des Tumeurs à cellules géantes
La tumeur à cellules géantes est une tumeur bénigne plus ou moins agressive localement capable de donner des métastases bénignes.
L'évolution sarcomateuse imprévisible par l'examen optique (1% des cas) correspond pour une large part à l'insuffisance fondamentale de l'examen morphologique et pour une faible part à une réelle transformation maligne. (Mazabraud 1994)
Dans notre relevé aucune tumeur à cellules géantes bénigne ne s'est transformé au fil des récidives pour devenir un sarcome riche en cellules géantes.
Par contre nous avons observé 4 cas de MFH riches en cellules géantes dont 2 n'ont exprimé leur malignité qu'à l'occasion de récidives itératives.
Dans tous les cas le réexamen des coupes histologiques initiales a redressé le diagnostic.
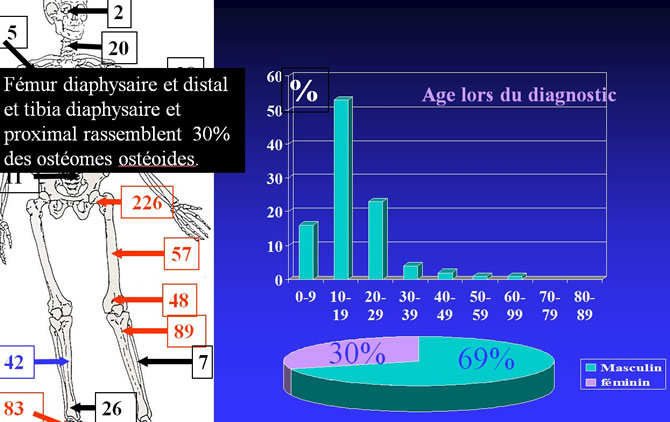
Répartition par sexe, topographies et age de 836 Ostéomes ostéoides
Fémur diaphysaire et distal et tibia diaphysaire et proximal rassemblent 30% des ostéomes ostéoides.
 Le Nidus
Le Nidus
 Aspect radiologique
Aspect radiologique
Dans la corticale condensée, le nidus (petite lacune).
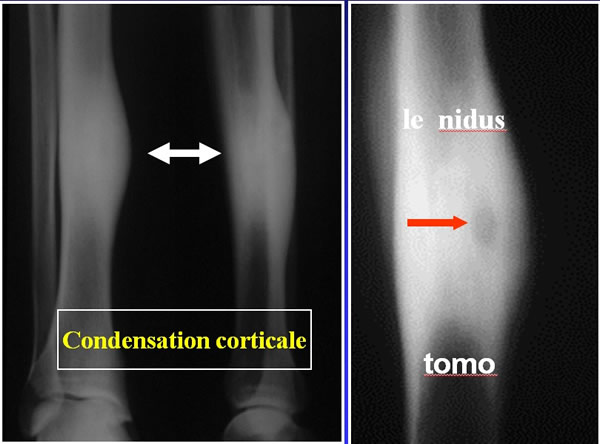 Intérêt de l'IRM
Intérêt de l'IRM
Chez certain malade le nidus n'est pas facile à mettre en évidence sur les radiographies standard.
C'est dans ces cas que le scanner et l'IRM peuvent être très utiles.
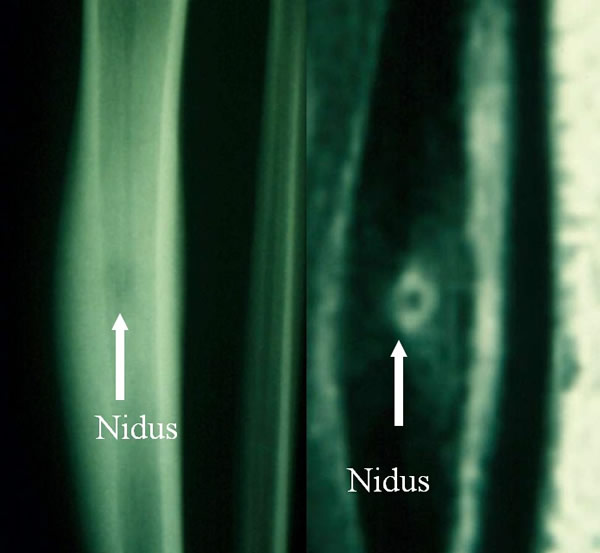 Ostéome ostéoide du fémur chez une jeune fille de 17 ans
Ostéome ostéoide du fémur chez une jeune fille de 17 ans
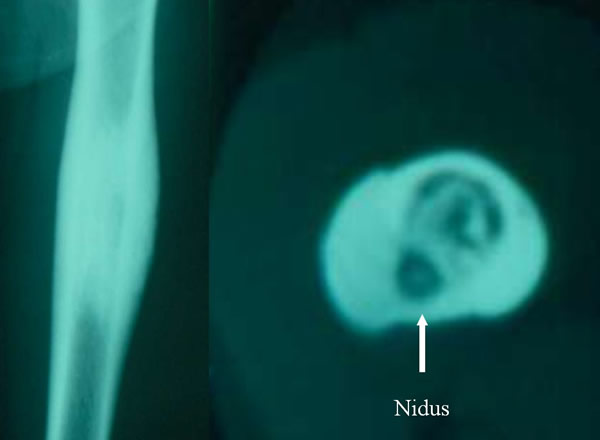 Aspect radiologique et TDM du nidus
Aspect radiologique et TDM du nidus
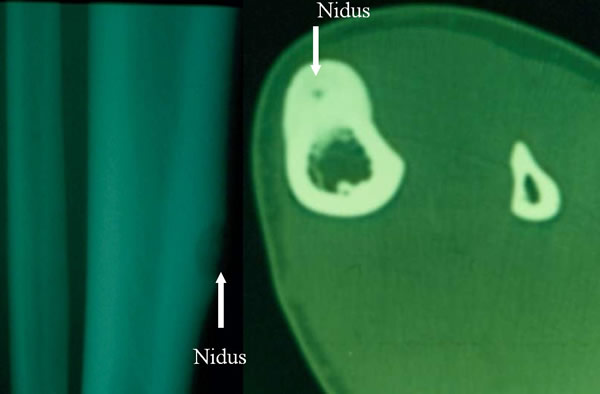 Ostéome ostéoide de la crête tibiale antérieure chez une femme de 32 ans
Ostéome ostéoide de la crête tibiale antérieure chez une femme de 32 ans
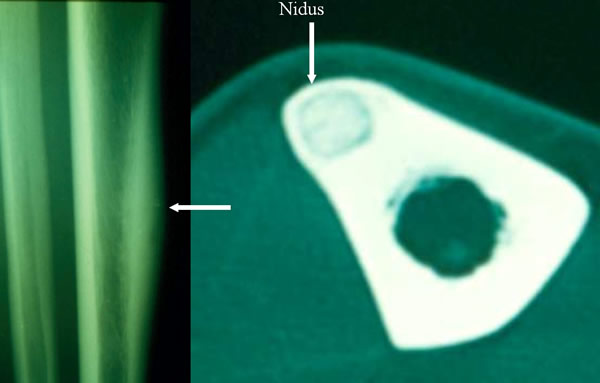 Traitement chirurgical classique
Traitement chirurgical classique
Ablation d'un volet cortical avec le nidus.
Risque de fracture Ostéosynthèse ? Greffe ? Reposition du volet après ablation du nidus ?
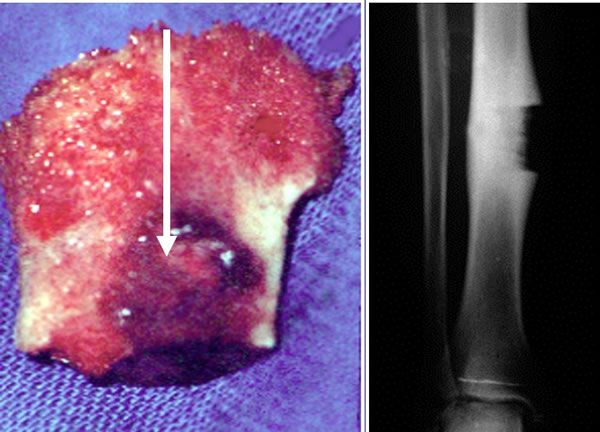 Traitement par résection et reconstruction par greffe spongieuse et plaque
Traitement par résection et reconstruction par greffe spongieuse et plaque
Le traitement classique par résection en bloc entraîne un défect osseux important et nécessite une prise de greffon et une ostéosynthèse augmentant ainsi le risque de complication et la durée de l'incapacité de travail.
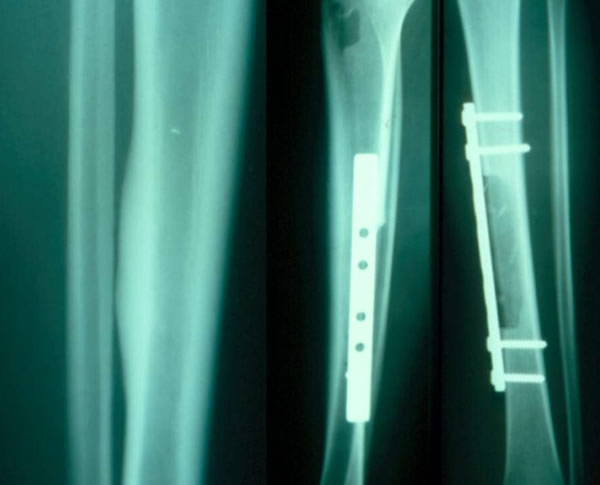 Traitement mini invasif
Traitement mini invasif
Ostéome ostéoide superficiel traité par mini ablation à la tréphine après repérage en scopie, permettant au malade de ne pas rester hospitalisé et de reprendre une activité professionnelle rapidement.
Le repérage per opératoire guidé par ordinateur récemment proposé paraît prometteur.
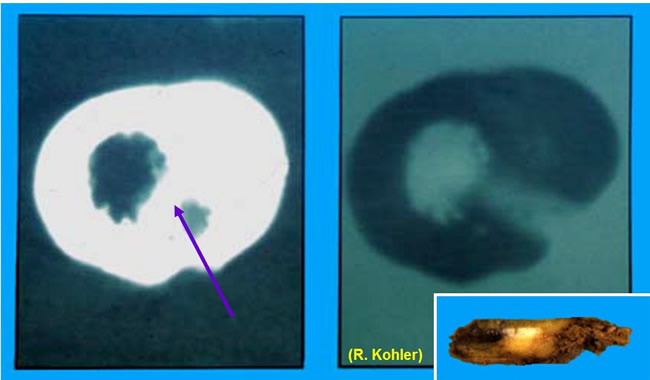
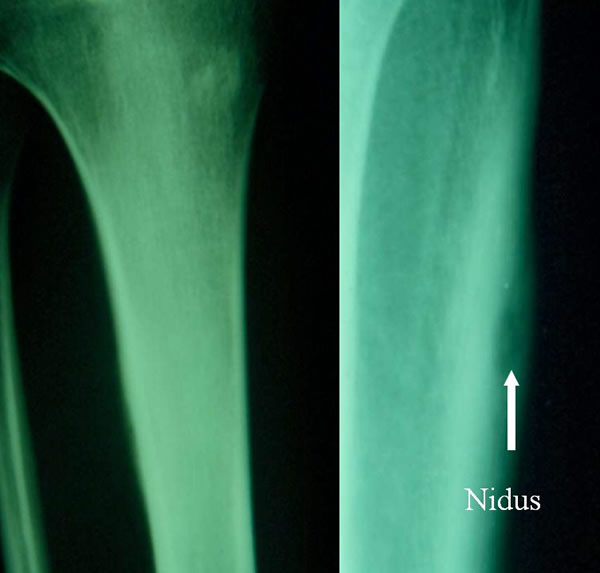 Forage Résection Osseuse Percutané (R. Kohler)
Forage Résection Osseuse Percutané (R. Kohler)
Repérage sous scanner et forage puis extraction des fragments.
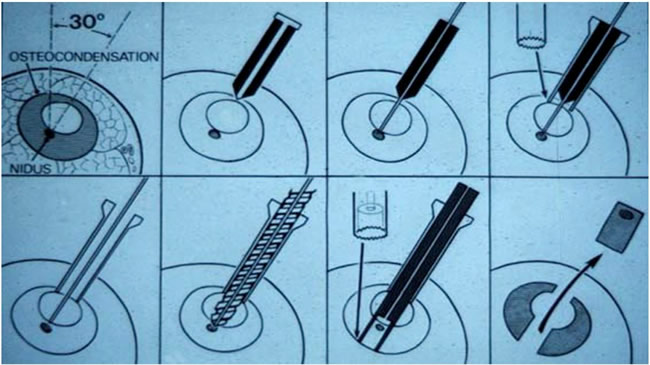
Matériel pour réaliser l'ablation du nidus.

Repérage et forage, puis récupération des fragments. Technique de choix pour les localisations difficiles d'accès. Examen anatomo-pathologique malheureusement impossible.
 Navigation fluoroscopique ?
Navigation fluoroscopique ?
La localisation de l'ostéome ostéoïde sur les radios simples est souvent peu aisée, ce qui génère des difficultés pour l'acte chirurgical.
L'utilisation du scanner pour le diagnostic et la navigation chirurgicale, permet le planning et la réussite d'un geste chirurgical non invasif.
L'utilisation de la navigation fluoroscopique peut permettre l'approche percutanée, avec simultanément une visualisation de face et de profil de bonne qualité sans irradiation excessive.
L'intérêt de la chirurgie assistée par ordinateur dans l'excision de l'Ostéome Ostéoïde. Navigation scannographique et fluoroscopique: 2 cas cliniques A.Eid MD; A.Badulescu MD; T.Martinez MD; P.Girard MD; P.Merloz MD - AOLF 2002
Navigation fluoroscopique : Radios standard
Femme agée de 48 ans : douleur du genou, impotence fonctionnelle, limitation d'amplitudes articulaires.
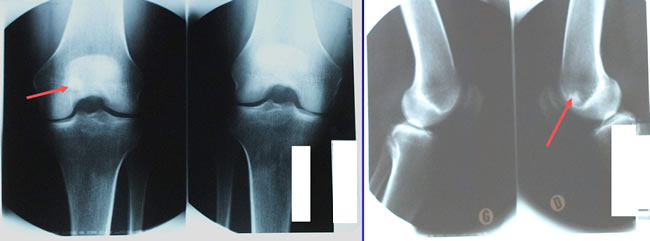
Radios des genoux face et profil - zone de condensation sur la face axiale du condyle médial du fémur droit.
L'intérêt de la chirurgie assistée par ordinateur dans l'excision de l'Ostéome Ostéoïde. Navigation scannographique et fluoroscopique: 2 cas cliniques A.Eid MD; A.Badulescu MD; T.Martinez MD; P.Girard MD; P.Merloz MD - AOLF 2002
Navigation fluoroscopique : IRM
Aspect tumoral du condyle fémoral interne.
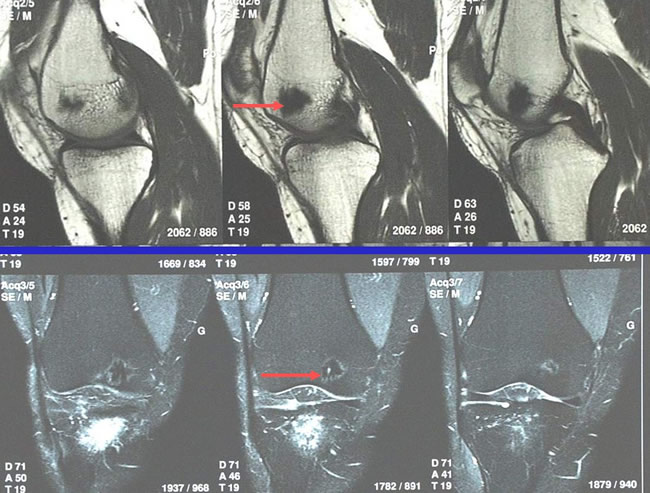 L'intérêt de la chirurgie assistée par ordinateur dans l'excision de l'Ostéome Ostéoïde. Navigation scannographique et fluoroscopique: 2 cas cliniques A.Eid MD; A.Badulescu MD; T.Martinez MD; P.Girard MD; P.Merloz MD - AOLF 2002
Navigation fluoroscopique : perop
L'intérêt de la chirurgie assistée par ordinateur dans l'excision de l'Ostéome Ostéoïde. Navigation scannographique et fluoroscopique: 2 cas cliniques A.Eid MD; A.Badulescu MD; T.Martinez MD; P.Girard MD; P.Merloz MD - AOLF 2002
Navigation fluoroscopique : perop
Aspect tumoral du condyle fémoral interne.
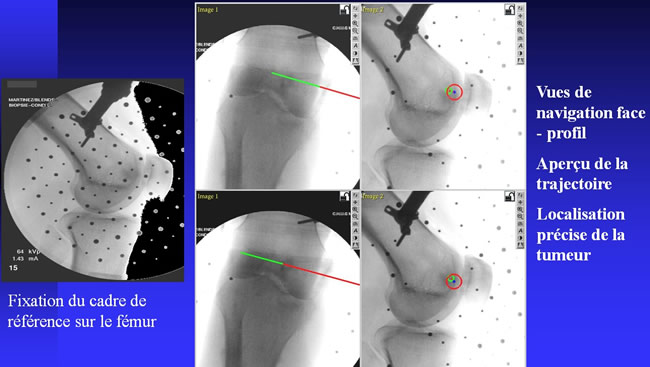 L'intérêt de la chirurgie assistée par ordinateur dans l'excision de l'Ostéome Ostéoïde. Navigation scannographique et fluoroscopique: 2 cas cliniques A.Eid MD; A.Badulescu MD; T.Martinez MD; P.Girard MD; P.Merloz MD - AOLF 2002
Résection complète de la tumeur avec comblement du trajet de résection par du phosphate tricalcique
L'intérêt de la chirurgie assistée par ordinateur dans l'excision de l'Ostéome Ostéoïde. Navigation scannographique et fluoroscopique: 2 cas cliniques A.Eid MD; A.Badulescu MD; T.Martinez MD; P.Girard MD; P.Merloz MD - AOLF 2002
Résection complète de la tumeur avec comblement du trajet de résection par du phosphate tricalcique
Navigation fluoroscopique - Rx postop.
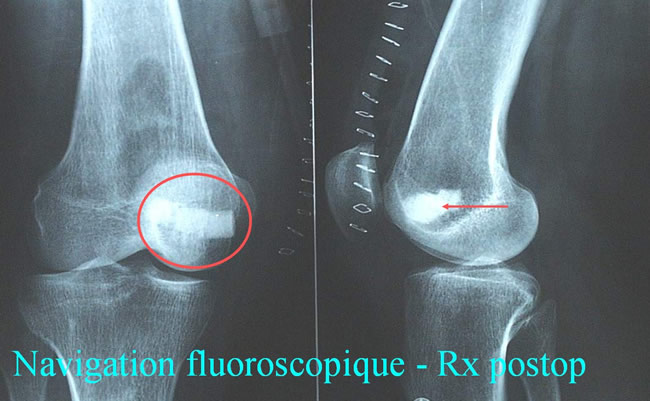 L'intérêt de la chirurgie assistée par ordinateur dans l'excision de l'Ostéome Ostéoïde. Navigation scannographique et fluoroscopique: 2 cas cliniques A.Eid MD; A.Badulescu MD; T.Martinez MD; P.Girard MD; P.Merloz MD - AOLF 2002
Navigation fluoroscopique - Scanner postop
L'intérêt de la chirurgie assistée par ordinateur dans l'excision de l'Ostéome Ostéoïde. Navigation scannographique et fluoroscopique: 2 cas cliniques A.Eid MD; A.Badulescu MD; T.Martinez MD; P.Girard MD; P.Merloz MD - AOLF 2002
Navigation fluoroscopique - Scanner postop
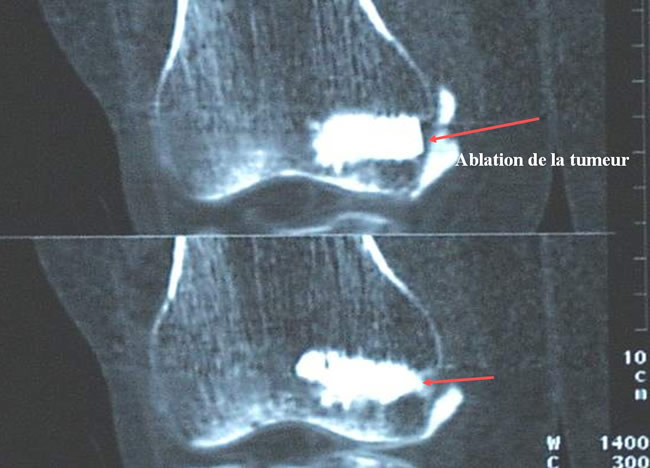 Navigation fluoroscopique Résultats
Navigation fluoroscopique Résultats
L'ablation de l'ostéome ostéoïde complète à été documentée par des images radio et scanner post-opératoires.
La douleur et la boiterie ont disparu en post-opératoire.
Pas de signes cliniques et radio-scannographiques de récidive tumorale à 6 mois et à un an.
Une courte période d'hospitalisation.
Dysplasies pseudo tumorales osseuses du genou
Fibrome non ossifiant, Kyste anévrysmal, Granulome éosinophile, Dysplasie fibreuse, Kyste solitaire
Répartition par sexe, topographies et age de 406 Fibromes non ossifiant
 Aspect radiologique typique
Aspect radiologique typique
Lacune claire sous corticale, métaphysaire bien limitée par un liseré de condensation découverte fortuite chez un adolescent.
Pas de réaction périostée.
Diagnostic évident.
Biopsie inutile.
Représente l'une des exceptions licites à la biopsie.
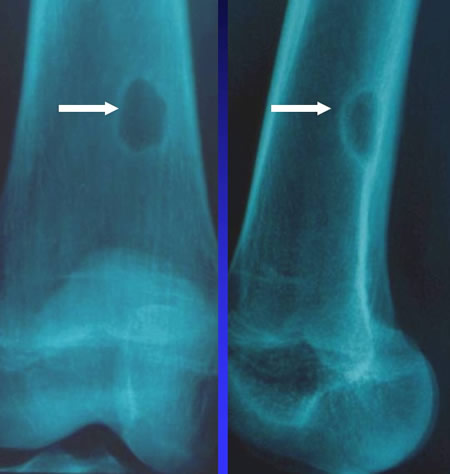 Cortical defect du fémur inférieur
Cortical defect du fémur inférieur
Découverte fortuite d'une lacune polycyclique sous corticale postérieure du fémur métaphysaire inférieure.
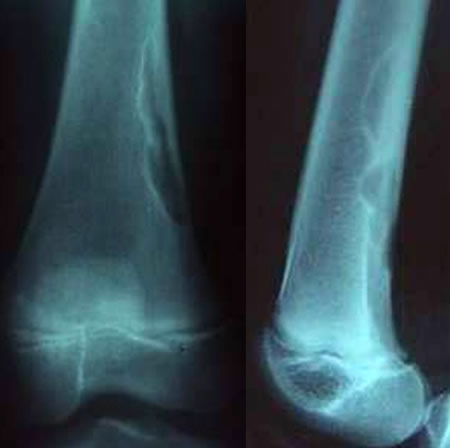 Autre Cortical defect du fémur inférieur
Autre Cortical defect du fémur inférieur
Scanner montrant bien le caractère polycyclique et bien limité de la lacune qui érode la corticale.
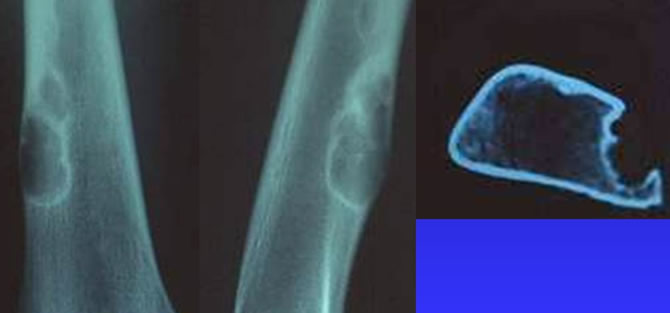 Évolution spontanée
Évolution spontanée
Bénigne. Guérison spontanée le plus souvent avec parfois "hyper guérison" aboutissant à une plage de condensation résiduelle.
Exceptionnellement le fibrome augmente de volume et menace de fracture.
Évolution naturelle d'un fibrome non ossifiant
Régression spontanée en 6 mois.
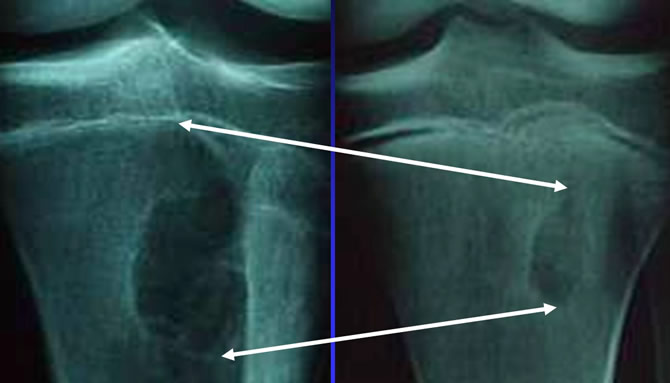 Régression spontanée d'un CD Tibial
Régression spontanée d'un CD Tibial
Régression spontanée en 9 mois.
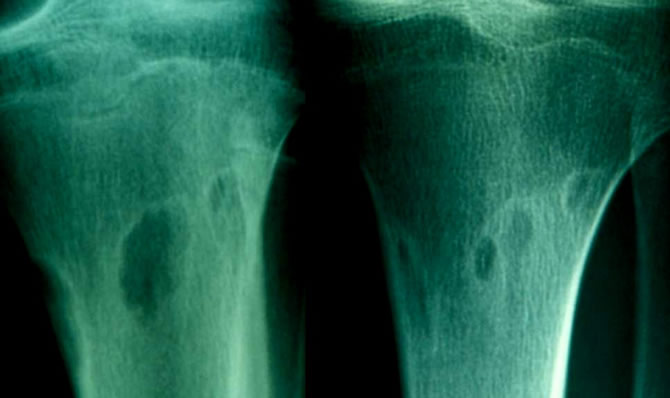 Hyper guérison d'un fibromes non ossifiant
Hyper guérison d'un fibromes non ossifiant
Certains fibromes non ossifiant guérissent en dépassant l'ossification normale de la zone osseuse malade. Aboutissant à une plage d'hyper densité d'ostéome.
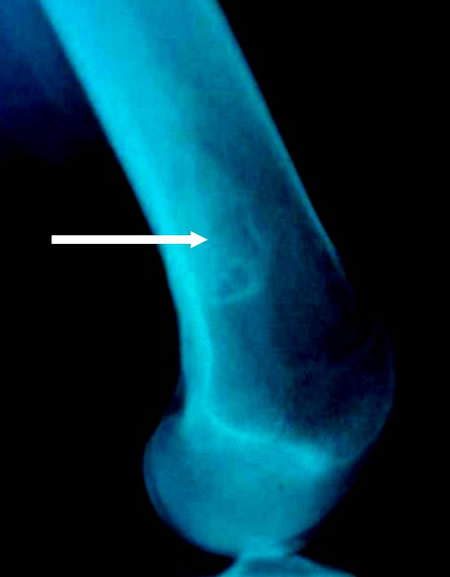 Poussée évolutive menaçant de fracture
Poussée évolutive menaçant de fracture
Aggravation nette de la plage d'ostéolyse évoluant vers la forme géante du fibrome non ossifiant.
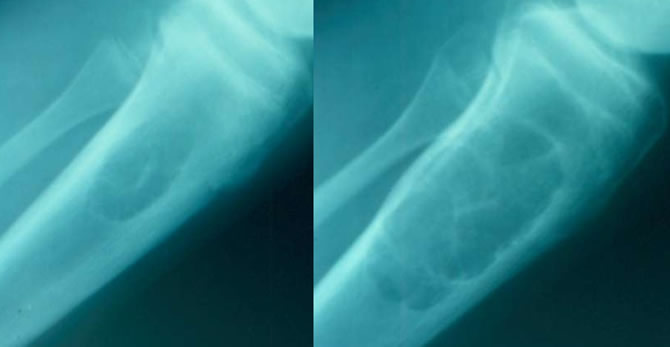 Evolution
Evolution
Bénigne. Guérison spontanée le plus souvent.
Les fractures pathologiques rares guérissent habituellement avec le traitement orthopédique.
Parfois intervention de curettage pour prévenir une fracture ou pour la stabiliser (pour l'EI du tibia surtout).
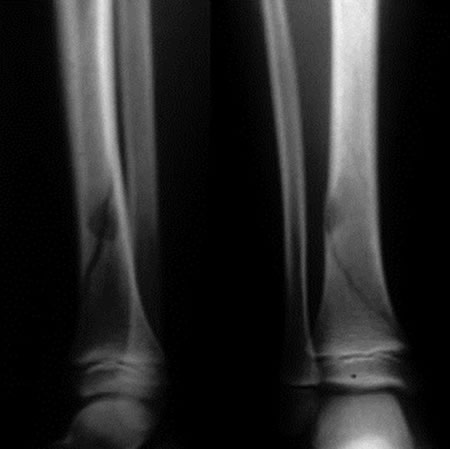 Guérison après curettage comblement
Guérison après curettage comblement
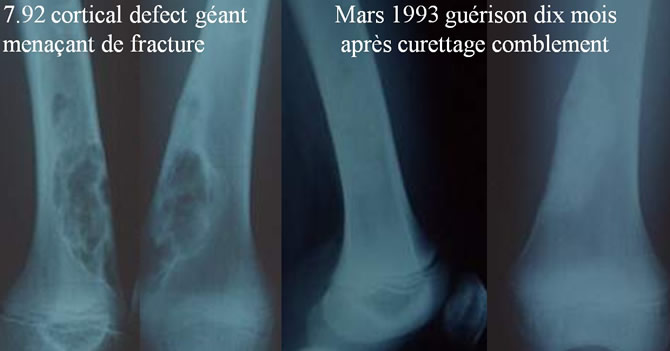 L'erreur à ne pas commettre !
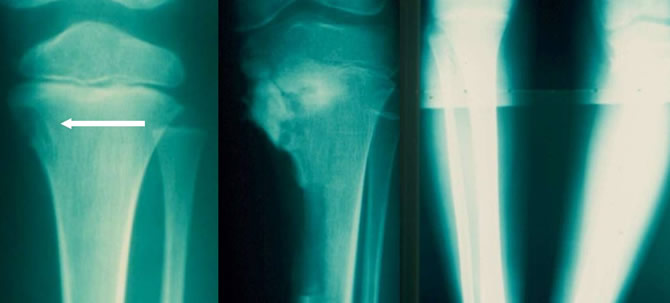
L'erreur à ne pas commettre !
Petit fibrome non ossifiant du tibia.
Biopsie large touchant le cartilage de conjugaison.
Gros varus apparu en 2 ans.
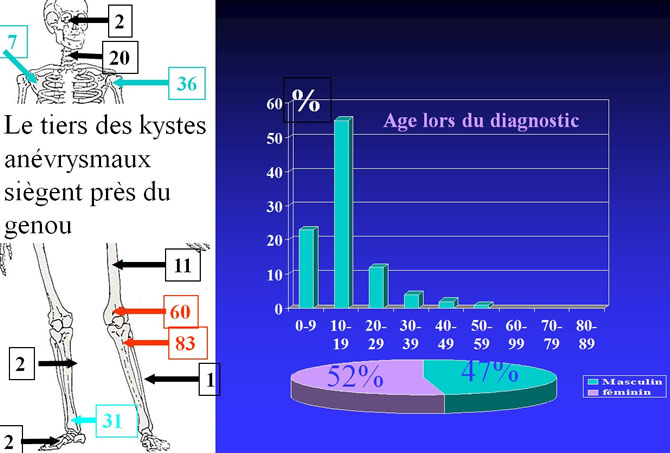
 Répartition par sexe, topographies et age de 569 Kystes Anévrysmaux
Répartition par sexe, topographies et age de 569 Kystes Anévrysmaux
Le tiers des kystes anévrysmaux siègent près du genou.
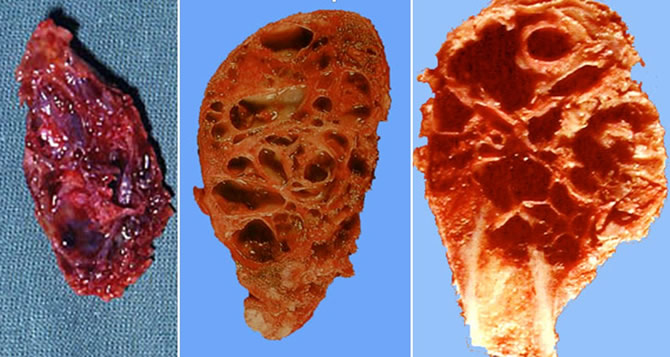
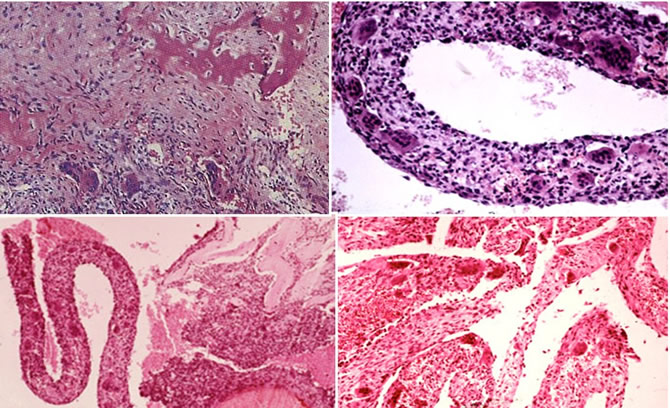
 Aspects macroscopiques
Aspects macroscopiques
Multiples cavités hématiques de quelques mm ou de 1 à 2 cm de diamètre contenant du sang non coagulé. Aspect en éponge.
 Aspects microscopiques
Aspects microscopiques
Les lacunes sont séparés par des cloisons conjonctives porteuses d'ostéoclastes et d'une ostéogenèse réactionnelle.
 Le signe le plus évocateur est la soufflure parfois extrême
Le signe le plus évocateur est la soufflure parfois extrême
Lacune ovalaire plus ou moins réticulée soufflant la corticale. Soufflure majeure par une tumeur ostéolytique parcourue de cloisons de refend.
Corticale amincie et même rompue par endroits mais sans éperon périosté.
Refoulement des parties molles par une mince coquille d'oeuf.
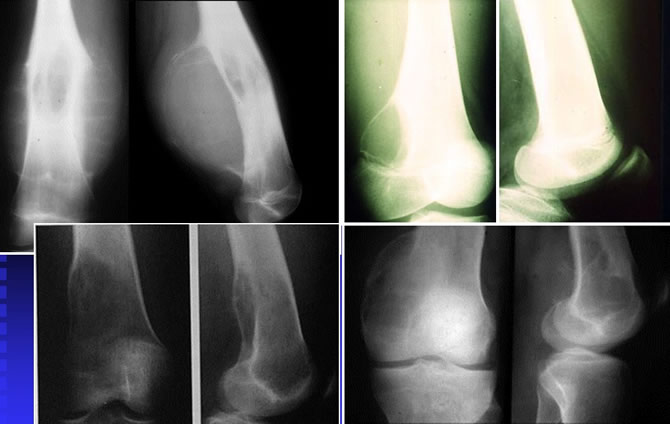
 Aspects de Kystes Anévrysmaux fémoraux
Aspects de Kystes Anévrysmaux fémoraux
Lésion centrale, parfois périphérique à développement sous périosté. Dimension : 2 à 25 cm.
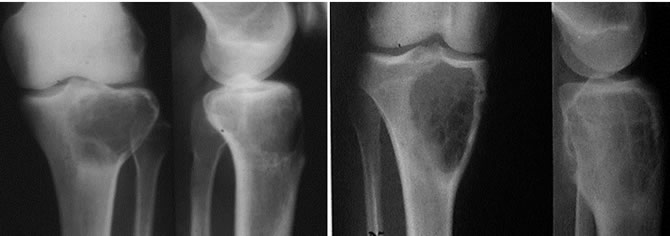
 Aspects de Kystes Anévrysmaux du tibia
Aspects de Kystes Anévrysmaux du tibia
Lacune ovalaire plus ou moins réticulée soufflant la corticale.
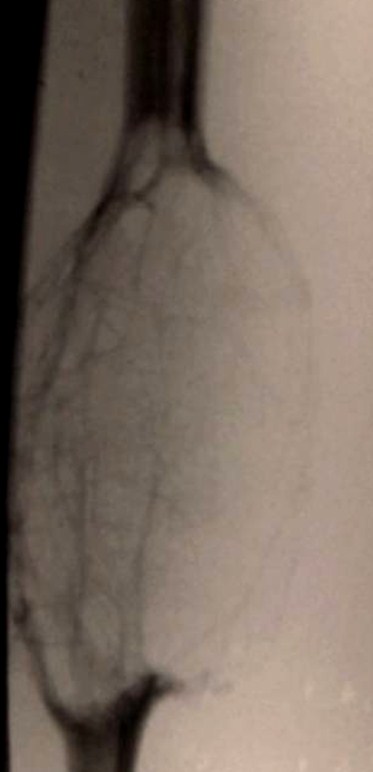
 L'expansion dans les parties molles peut être prédominante et trompeuse
L'expansion dans les parties molles peut être prédominante et trompeuse
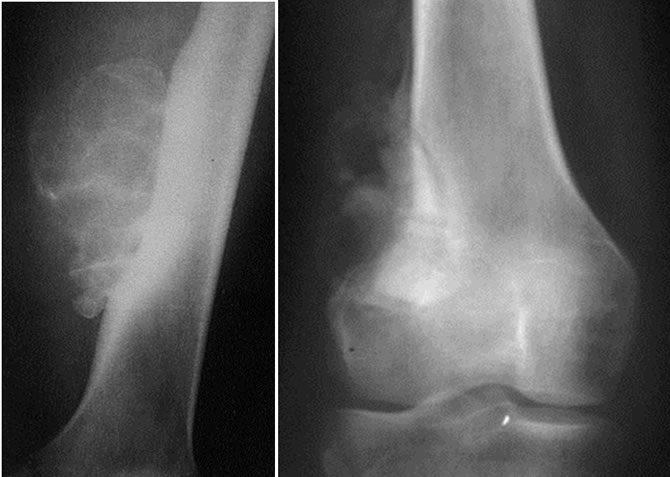 Bilan d'extension locale : Le scanner
Bilan d'extension locale : Le scanner
Le scanner montre parfois des niveaux liquides précise les limites en coquille d'oeuf.
La scintigraphie est modérément positive.
L'artériographie ou l'angio IRM montre les pédicules artériels et permet de discuter une embolisation.
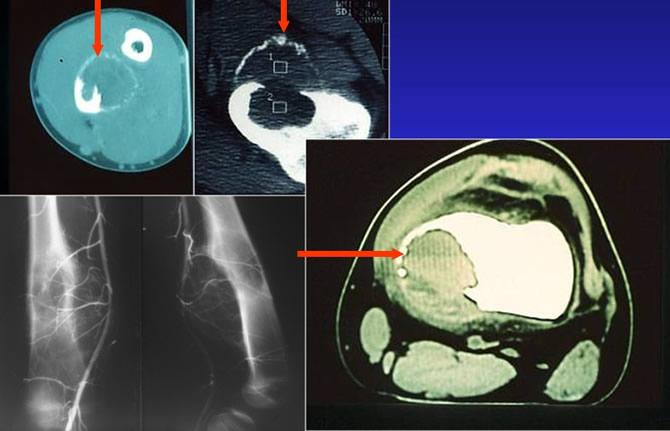 Diagnostic différentiel : sarcome d'Ewing
Diagnostic différentiel : sarcome d'Ewing
Soufflure globale de l'os.
Amincissement cortical majeur.
Ossifications dans les parties molles.
peuvent évoquer une tumeur maligne.
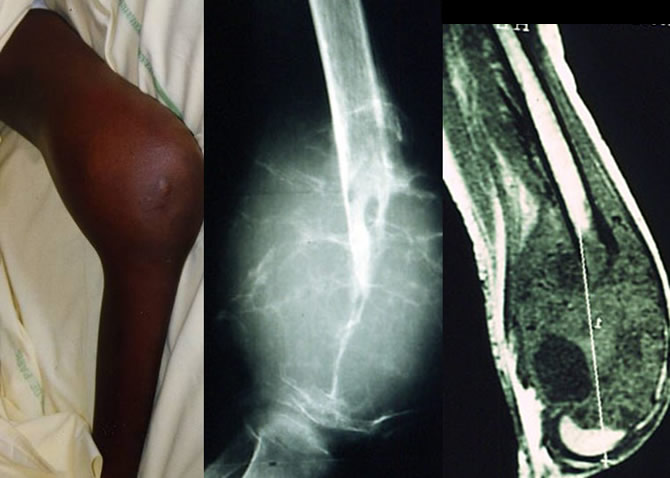
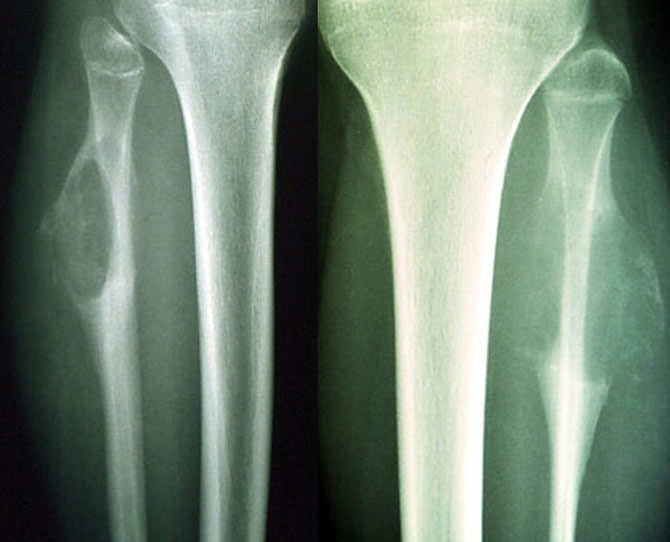 Diagnostic différentiel : ostéosarcome
Diagnostic différentiel : ostéosarcome
Jeune fille de 13 ans souffrant depuis 6 mois de son genou gauche. Tuméfaction apparue il y a 3mois. Fracture spontanée.
 TRAITEMENT du KYSTE ANÉVRYSMAL
TRAITEMENT du KYSTE ANÉVRYSMAL
La biopsie est indispensable pour faire le diagnostic.
La simple surveillance basée sur la rare régression spontanée de Kystes Anévrysmaux ne se justifie que rarement.
Curetage + comblement au niveau des os longs porteurs avec ostéosynthèse en cas de fragilité.
Résection pour les os accessoires (péroné...)
Résection et reconstruction pour les cas où le simple curetage est insuffisant.
La radiothérapie ne doit plus être utilisée même dans les curetages insuffisants ou les récidives (cancers radio induits).
L'embolisation permet de préparer la chirurgie dans les localisations fémorales hautes difficiles à opérer.
Le curetage comblement constitue le traitement de choix
La biopsie préalable est indispensable pour faire le diagnostic.
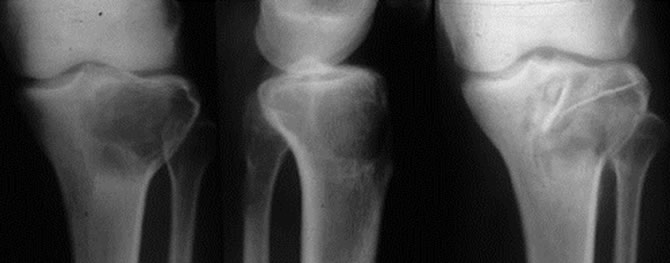 Guérison après Curetage + comblement
Guérison après Curetage + comblement
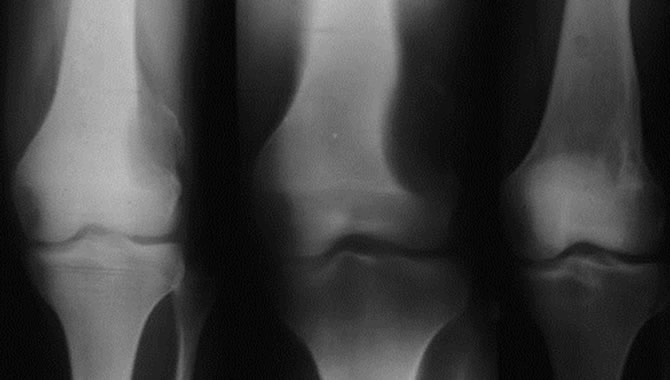 Évolution après curettages comblements répétés d'un kyste anévrysmal
Évolution après curettages comblements répétés d'un kyste anévrysmal
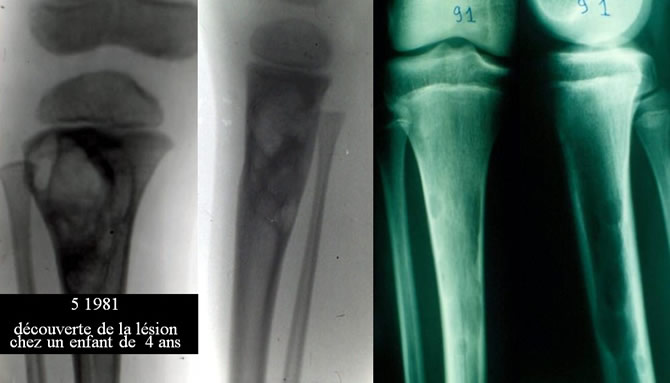 Ostéosynthèse et comblement d'une lésion préfracturaire
Ostéosynthèse et comblement d'une lésion préfracturaire
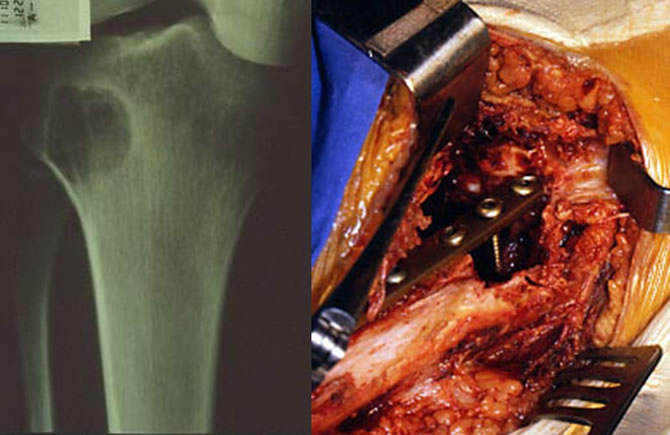 Curetage, comblement + ostéosynthèse
Curetage, comblement + ostéosynthèse
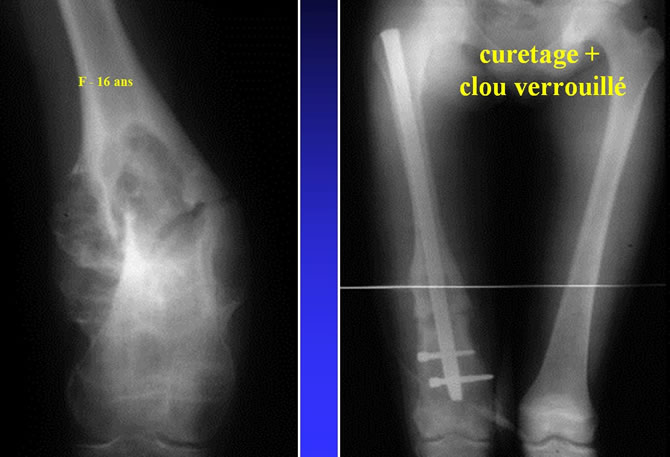 Embrochage d'un kyste anévrysmal Enfant de 9 ans
Embrochage d'un kyste anévrysmal Enfant de 9 ans
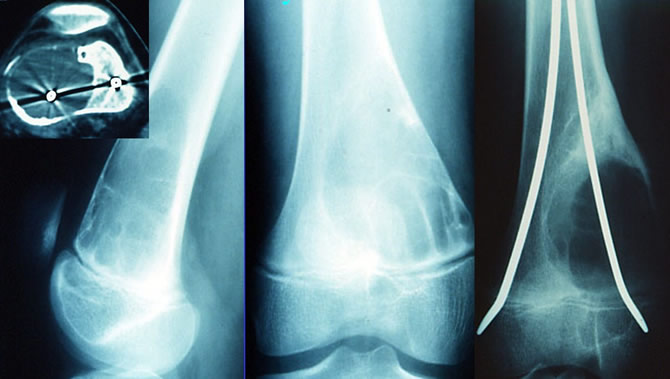 Granulome éosinophile de l'os
Granulome éosinophile de l'os
L'atteinte du genou est rare (4%). Une nette prédominance masculine est retrouvée dans toutes les séries publiées. Le sexe ratio moyen est proche de 2.
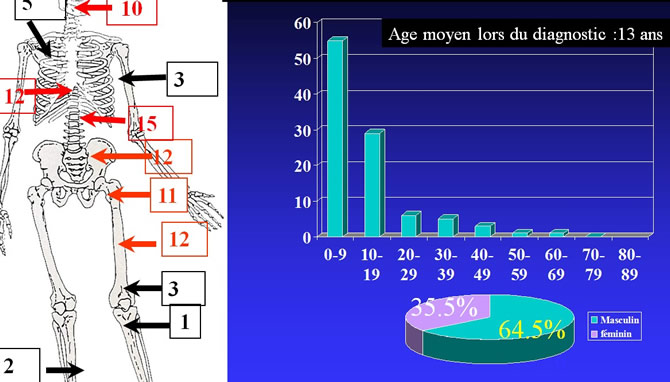 La diaphyse fémorale représente la première localisation des os longs
La diaphyse fémorale représente la première localisation des os longs
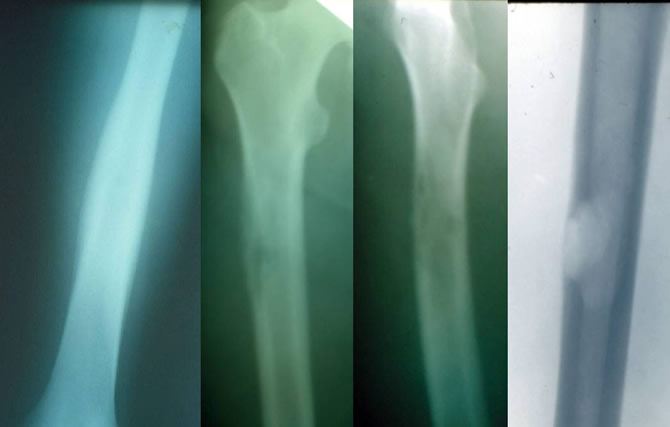 Localisation fémorale inférieure
Localisation fémorale inférieure
Lacune géométrique à limites nettes très évocatrice.
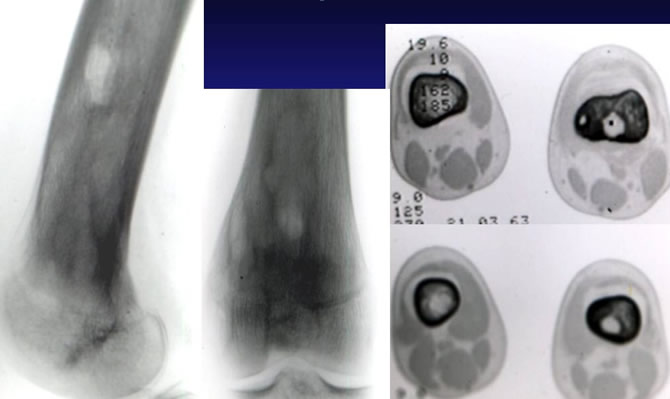 Localisation tibiale
Localisation tibiale
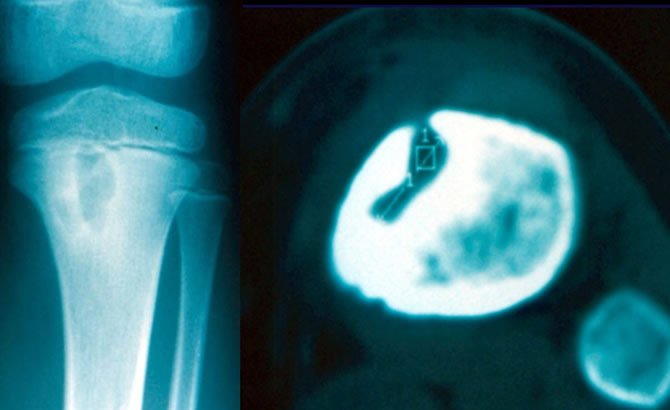 Localisation péronière
Localisation péronière
Gros envahissement des parties molles.
Les localisations aux os distaux sont relativement rares.Lorsqu'elle s'accompagnent d'un volumineux envahissement des parties moles comme dans cette observation elles peuvent faire craindre le sarcome.
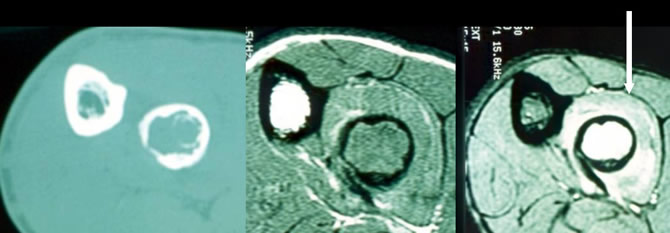 L'atteinte des parties molles peut être volumineuse
L'atteinte des parties molles peut être volumineuse
Grosse atteinte des parties molles autour d'une localisation fémorale distale unique chez un garçon de 11 ans.
Elle doit faire craindre une tumeur maligne primitive.
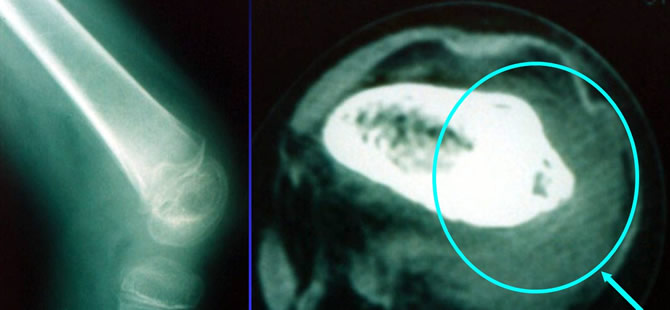 La biopsie
La biopsie
La biopsie est indispensable au diagnostique.
Dans certains cas la biopsie à l'aiguille peut suffire.
Dans les cas profonds ou difficile la biopsie chirurgicale s'impose après avoir prévenu l'anatomopathologiste.
L'examen bactériologique doit être systématique car il représente parfois un élément essentiel du diagnostic.
Aspect macroscopique du granulome éosinophile
Macroscopiquement le granulome est constitué de tissu mou gris jaune ou marron parsemé de plages hémorragiques ou nécrotiques.
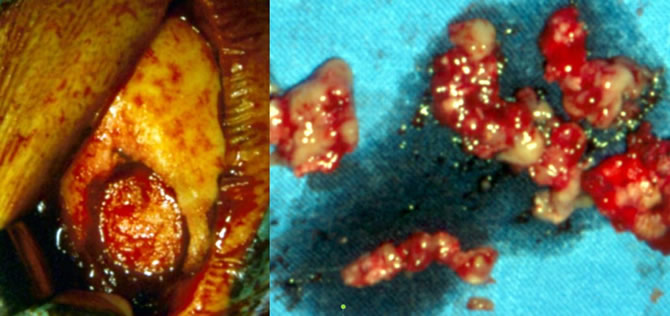 Aspect microscopique
Aspect microscopique
Dépendent du stade auquel est vue la maladie.
La tumeur est typiquement polymorphe constituée d'amas de cellules de Langherans infiltrées de polynucléaires éosinophiles et de plages de nécrose.
Les cellules de Langherans ont un cytoplasme volumineux faiblement éosinophile,souvent chargé de vacuoles et de granulations.Le noyau est volontiers ovoïde, ou réniforme,encoché à contours parfois tourmentés.
Les granulocytes sont tantôt très abondants tantôt rares ou même absents.
Diagnostic différentiel
Les variations considérables de l'aspect microscopique ne permettent pas toujours une certitude diagnostique en particulier en cas d'absence de granulocytes éosinophiles.
La richesse en polynucléaires, l'absence de nécrose ou d'histiocytes peuvent évoquer une infection ou une tumeur (hodgkin, sarcome histiocytaire...).
Les techniques de marquage immunologique peuvent alors se révéler précieuses :
Antigène Protéine S100 et CD1
Anticorps CD68 , CD1 , et parfois CD4
Marqueur des corps de Birbeck
Évolution du granulome éosinophile de l'os
Les atteintes des maxillaire exposent parfois aux pertes dentaires.
Les localisations rachidiennes peuvent très exceptionnellement comprimer les structures nerveuses et entraîner des déficits neurologiques.
Les grandes lacunes des os longs se compliquent très rarement de fracture.
Le granulome éosinophile du genou apparaît donc comme une maladie globalement bénigne.
Le traitement doit donc surtout ne pas nuire.
Les moyens thérapeutiques et indications (1)
Le curettage biopsie suffit dans la majorité des cas à guérir la localisation osseuse.
Lorsque la perte de substance est importante un comblement s'impose, voire une ostéosynthèse.
Certaines localisations restent évolutives ou douloureuses ; les infiltrations du foyer par des corticoïdes au besoin répétées permettent habituellement de les guérir.
Les petits os douloureux peuvent faire préférer la résection.
Traitement par curettage-comblement
Localisation métaphysaire supérieure du péroné chez un jeune enfant responsable de douleurs importantes.
Biopsie, curettage et comblement en un temps.
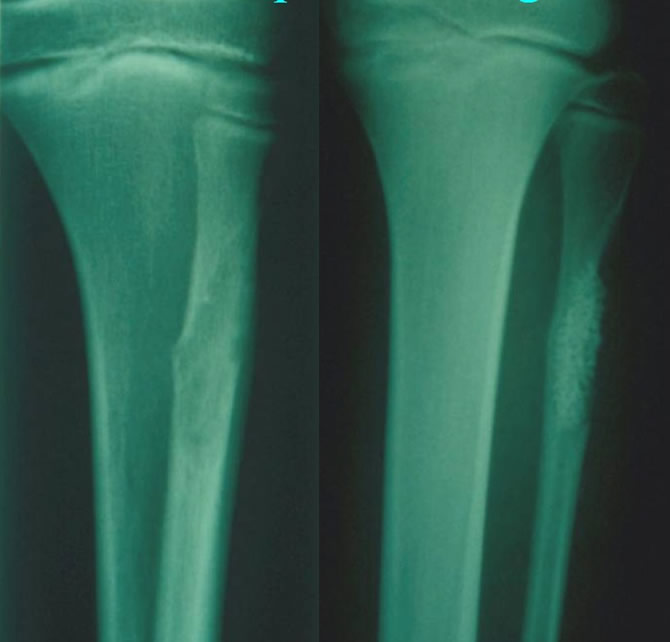 Répartition par sexe, age et topographies de 347 dysplasies fibreuses
Répartition par sexe, age et topographies de 347 dysplasies fibreuses
Le genou regroupe environ un tiers des cas.
 Dysplasie fibreuse
Dysplasie fibreuse
Constituée de tissus fibreux et osseux mal formé, la dysplasie fibreuse peut être monoostotique ou plurifocale et faire alors parties du syndrome d'Albright (taches café au lait+dysfonction endocrinienne) ou du syndrome de mazabraud (associée à des myxomes).
Seule les localisations solitaires peuvent être considérées comme des pseudotumeurs.
Elle commence toujours avant la puberté mais les lésions asymptomatiques peuvent être découverte à tout age.
Aspects radiologiques de la dysplasie fibreuse
Lésion intramédullaire apparue chez l'enfant et progressivement croissante soufflant fréquemment l'os porteur.
La matrice lésionnelle constituée d'os immature prend volontiers l'aspect en "verre dépoli" contenant parfois quelques lobules cartilagineux.
Lorsque la lésion est immature l'aspect radiologique peut être lytique pur.
Les limites de la lésion sont toujours bien nettes et parfois cernées d'une ligne de condensation.
Les corticales adjacentes peuvent être amincies ou soufflées mais restent continues.
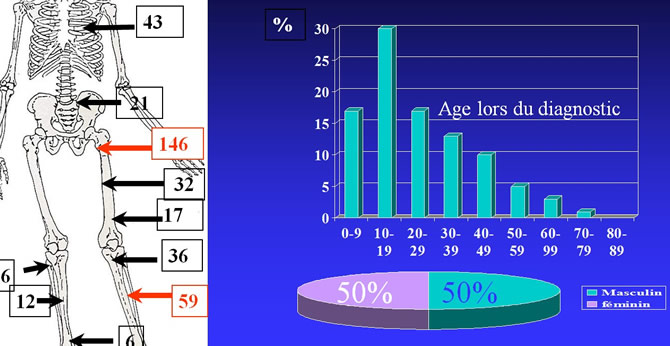
Homme de 25 ans
Lésion révélée par l'apparition indolore d'une bosse de la crête tibiale antérieure.
Limites nettes.
Ostéolyse pure.
Corticales respectées
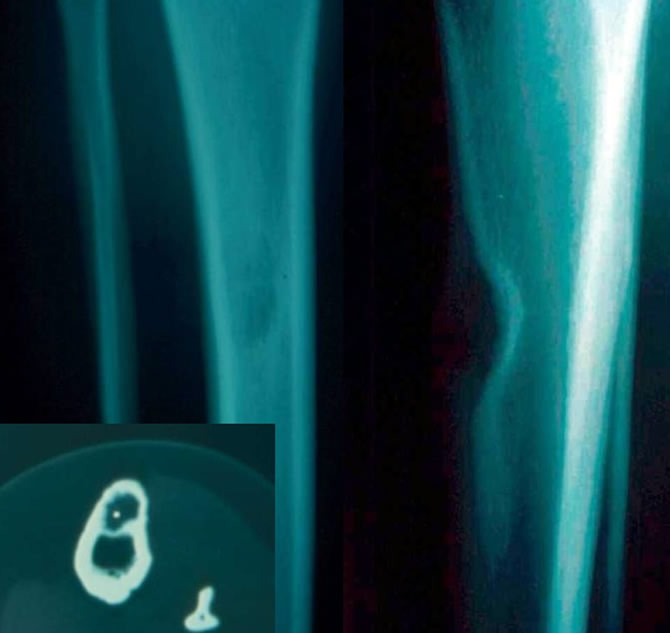 Jeune fille de 15 ans
Jeune fille de 15 ans
Lésion lytique rapidement croissante agressive ,menaçant de fracture.
Limites lésionnelles bien dessinées mais destruction corticale importante.
Scanner confirmant la continuité corticale et l'absence d'atteinte des parties molles.
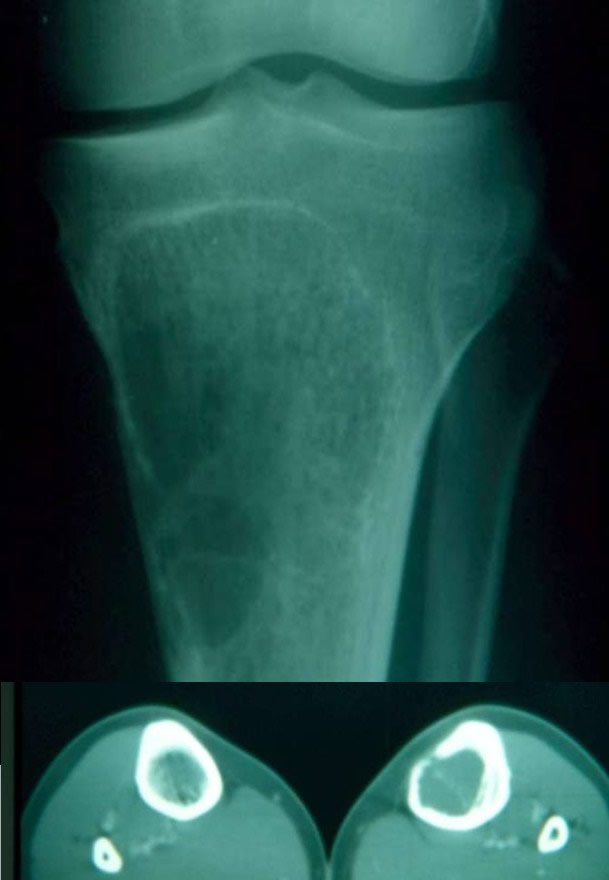 Évolution après résection allogreffe
Évolution après résection allogreffe
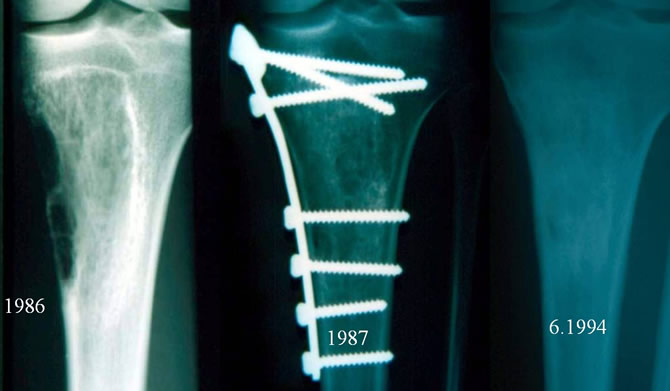 Jeune femme de 35 ans
Jeune femme de 35 ans
Image lacunaire bien limitée avec matrice en verre dépoli.
Scanner montrant le respect des corticales.
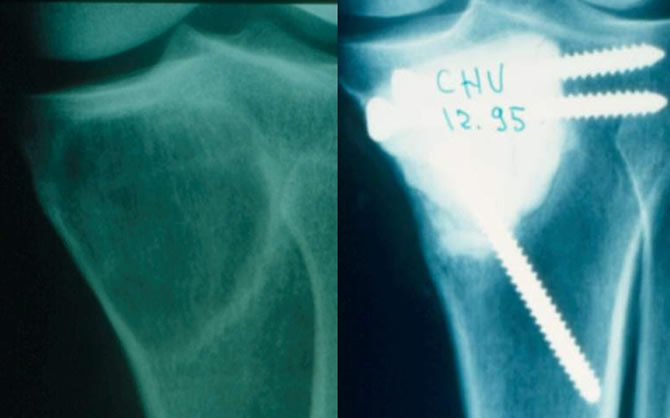
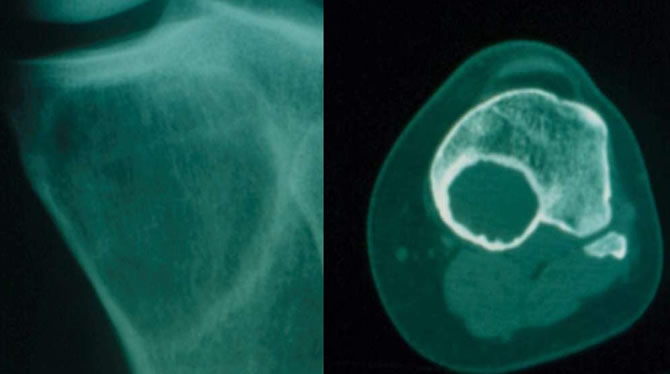 Évolution après curettage comblement ciment
Évolution après curettage comblement ciment
Biopsie : dysplasie fibreuse.
Curettage Comblement ciment Ostéosynthèse.
Après huit ans genou cliniquement normal. Radiographies ne montrant aucune modification autour du bloc de ciment. Interligne articulaire sus jacent normal.
 Répartition par sexe, topographies et age de 987 Kystes Solitaires
Répartition par sexe, topographies et age de 987 Kystes Solitaires
Moins de 5% des kystes solitaires siègent près du genou.
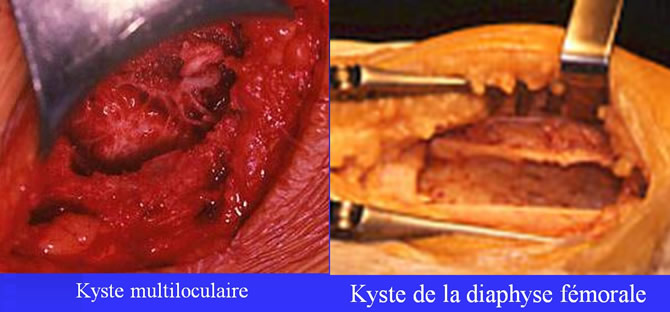
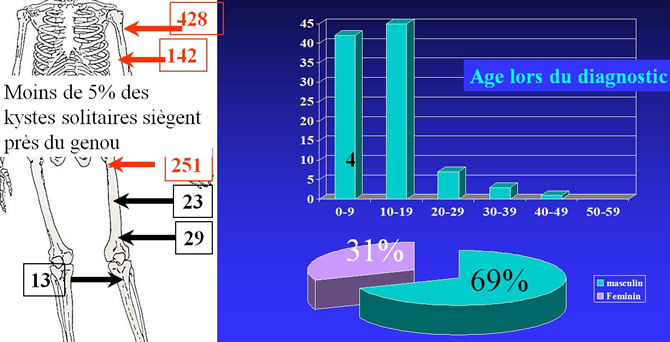 Aspect macroscopique des KYSTES OSSEUX
Aspect macroscopique des KYSTES OSSEUX
La cavité a des parois fines et contient un liquide citrin ou séro-hématique 1 membrane conjonctive tapisse la cavité.
Au pôle inférieur : lamelle plus dure
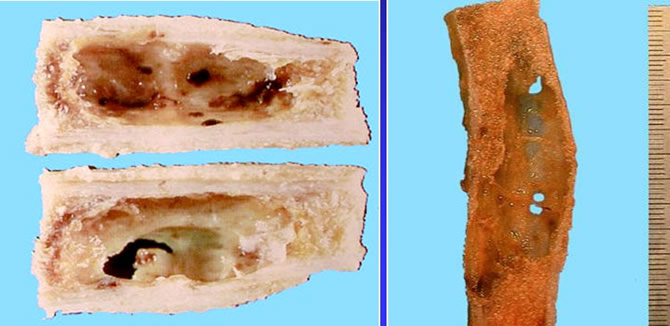 Biopsie des KYSTES OSSEUX ?
Biopsie des KYSTES OSSEUX ?
Biopsie : non indispensable au diagnostic (Biopsie quand on a d'autres raisons d'opérer)
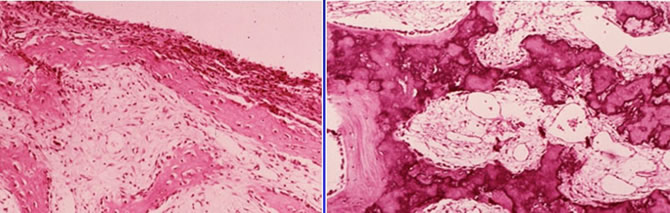 Aspect radiologique du kyste osseux
Aspect radiologique du kyste osseux
Dystrophie pseudo tumorale unique.
Lytique pure métaphysaire ou métaphyso diaphysaire.
Centrale.
Bien limitée, corticales amincies mais respectées, pas de réaction périostée.
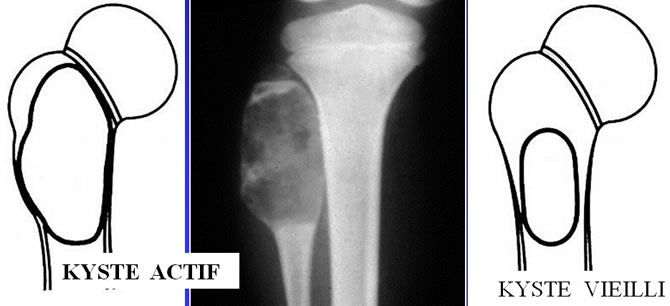 KYSTE SOLITAIRE VIEILLI
KYSTE SOLITAIRE VIEILLI
À distance du cartilage conjugal, Lytique, Bien limitée, De l'adolescent et adulte jeune, Habituellement asymptomatique.
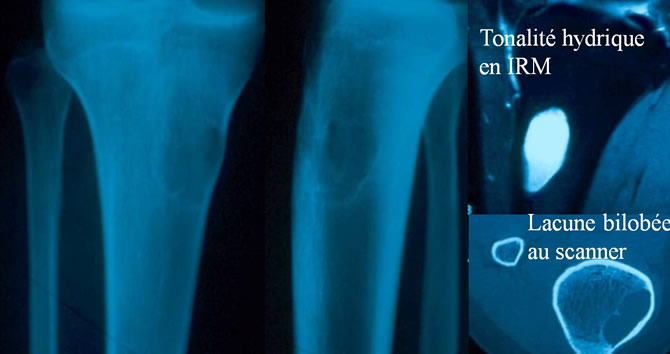 Le Kyste vieilli est une cavité vide
Le Kyste vieilli est une cavité vide
 TRAITEMENT des KYSTES OSSEUX
TRAITEMENT des KYSTES OSSEUX
Simple surveillance radiologique possible pour les kystes "inactifs" découverts après la fin de la croissance.
Injections locales de corticoïdes.
Sous AG, 2 trocarts, évacuation du liquide intra-kystique (40 à 80 mg d'acétate de méthylprednisolone).
Parfois, il faut prévenir ou traiter une fracture.
Attention aux cartilages de croissance !!
La surveillance radiologique est poursuivie jusqu'à la fin de la croissance. Récidive toujours possible.
Persistance, en général, d'une image lacunaire cicatricielle ou kyste résiduel Fragilisation et fractures possibles à l'âge adulte.
Conclusion
Chez l'enfant, une imagerie typique permet de porter le diagnostic dans un nombre limitée de cas :
- Exostose ostéogénique,
- Lacune corticale typique,
- Kyste solitaire non fracturé,
Dans les autres cas le diagnostic repose sur un faisceau d'arguments dont la biopsie constitue le principal.
Le diagnostic d'une tumeur osseuse bénigne repose le plus souvent sur un faisceau d'arguments dont la biopsie constitue le principal.
Si la malignité ne peut être exclue, CE GESTE TROP SOUVENT CONSIDERE COMME MINEUR DOIT ETRE REALISE PAR L'OPERATEUR RESPONSABLE DE LA RESECTION ULTERIEURE APRES SCANNER ET/OU IRM ET CONCEPTION DU GESTE DEFINITIF.


