|
|
 |
 |
 |
 |

Publié sur :
La Médecine Infantile N°1 Janvier 1983 (Maloine S.A. édit.) - 1983 Voir la version PDF de cette publication : 
Dysplasie fibreuse monoostotique
Nicole Delépine, Gérard Delépine, J.C. Desbois, F. Grétillat
Dysplasie fibreuse monoostotique
Maladie de l'ossification du squelette, la dysplasie fibreuse pose des problèmes diagnostiques et thérapeutiques bien différents selon sa présentation diffuse ou solitaire. Nous n'envisagerons ici que les formes localisées, pseudo-tumorales, de la
maladie.
ÉTIOLOGIE
1) Fréquence : la dysplasie fibreuse monoostotique est peu fréquente. A peine plus de 800 observations en ont été rapportées, isolément ou dans des séries (11, 13, 16, 17, 20, 26, 36, 37) dont très peu rassemblent plus de 50 cas. Elle représente environ 2% des tumeurs osseuses primitives des principaux relevés ; sa fréquence réelle est cependant vraisemblablement supérieure car son évolution souvent asymptomatique n'incite guère à consulter en milieu spécialisé.
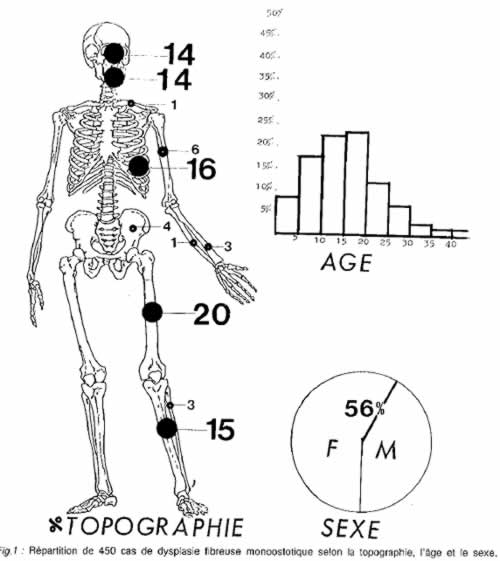
2) Age : l'apparition précoce de la maladie est soulignée par toutes les séries. Lors du diagnostic, la moitié des malades ont moins de 15 ans. Cependant, contrairement aux formes diffuses, les atteintes monoostotiques se manifestent rarement avant 3 ans.
3) Sexe : la plupart des séries observent une légère prédominance féminine. Le sex-ratio est proche de 0,80.
4) Siège : tous les os peuvent être atteints mais la dysplasie fibreuse localisée, pseudo tumorale, touche électivement les gros os longs (fémur, tibia, humérus) et les os plats (côtes, face, mandibule). L'atteinte du bassin et des petits os des extrémités, fréquente dans les formes polyostotiques, est rare dans les formes localisées. Sur les os longs, la dysplasie fibreuse est habituellement métaphysaire ou diaphysaire ; la localisation épiphysaire, exceptionnelle, est cependant possible (23).
DIAGNOSTIC
1) Les circonstances révélatrices (26, 11, 16, 32, 17, 13, 36) : les foyers solitaires de dysplasie fibreuse n'entraînent habituellement qu'un minimum de signes. Près de 40 % des cas sont ainsi révélés par une fracture pathologique et 20 % par un examen radiographique fortuit. Ailleurs, c'est une discrète douleur osseuse avec sensibilité locale exacerbée ou une déformation progressive qui attirent l'attention.
2) L'examen radiographique est essentiel (18, 3, 32, 17, 13, 36, 39, 8, 11) : l'image réalisée dépend de la quantité de tissu fibreux, de l'abondance de l'os néoformé et de son degré de calcification.
a) L'ostéolyse est habituellement prédominante. Elle objective le remplacement de l'os normal par le tissu fibreux. Elle réalise des lacunes assez bien limitées, à point de départ centro-médullaire, arrondies ou ovalaires. Souvent multiples, ces lacunes peuvent confluer donnant un aspect aérolaire. De petits îlots osseux métaplasiques ponctuent parfois les lacunes de petites calcifications. L'ostéolyse à point de départ centra-médullaire s'étend en amincissant les corticales et en élargissant le canal médullaire.
b) Une condensation importante peut s'observer lorsque l'ostéoformation prédomine, c'est exceptionnel, en dehors des os plats de la face et des côtes (3, 39).
c) Il n'existe ni réaction périostée, ni rupture corticale, ni envahissement des parties molles, à moins qu'une fracture spontanée n'ait modifié l'aspect radiographique.
d) L'os atteint est habituellement déformé. Il est soufflé trois fois sur quatre. Il peut être courbe lorsqu'il est soumis à des contraintes mécaniques importantes (fémur, tibia, péroné).
3) Les examens de laboratoire ne sont d'aucun secours pour le diagnostic de ces formes mono-osseuses.
4) L'examen anatomo-patbologique est toujours indispensable.
a) Aspect macroscopique : lors de l'intervention le tissu dysplasique apparaît recouvert d'une coque osseuse qu'il lamine et distend progressivement. Le tissu fibreux est ferme, dense, peu vascularisé, jaunâtre ou grisâtre. Les limites d'avec l'os sain sont nettes et permettent un curetage facile.
b) L'examen histologique montre une prolifération de cellules fusiformes ou ovalaires, de taille réduite, disposées en nappes, sans mitoses nombreuses. La matrice collagène qu'elles sécrètent est ponctuée irrégulièrement de massifs ostéoïdes donnant un aspect d'ossification primitive. L'activité ostéoblastique est faible ou absente. Certains aspects lésionnels, associés inconstamment, ne doivent pas induire en erreur, qu'il s'agisse de foyers cartilagineux, de plages de xanthélasmisation, de kystisation, de cellules géantes, de lipophages... L'absence apparente de spécificité et l'association possible à d'autres tumeurs expliquent les difficultés fréquentes du diagnostic anatomique et soulignent la nécessité de replacer les données de l'examen histologique dans le contexte radioclinique et évolutif.
ÉVOLUTION
1) L'évolution spontanée est lente et longtemps asymptomatique. Elle se fait par poussées imprévisibles. La stabilisation des lésions à la puberté constitue la règle générale (13, 16,17, 26, 32, 36, 37).
2) Des complications mécaniques menacent les gros os longs. Les fractures spontanées, fréquentes et souvent révélatrices, sont habituellement peu déplacées ; elles consolident dans des délais normaux. Des incurvations des membres atteints peuvent apparaître après fractures itératives, lors de lésions très étendues, ou après troubles de croissance secondaires aux traumatismes répétés ; elles sont rares dans les formes monoostotiques.
3) Une reprise évolutive à l'âge adulte est toujours possible, parfois après 10ans d'accalmie, parfois apparemment déclenchée par une grossesse. Lorsque l'ostéolyse est trop rapidement croissante, elle doit faire craindre la dégénérescence.
4) La dégénérescence est en effet possible à l'âge adulte (1, 2, 4, 6, 9, 12, 14, 15, 19, 22, 24, 25, 27, 28, 29, 30, 31, 33, 34, 35, 38). En l'absence de données statistiques convergentes le risque d'évolution maligne est bien difficile à estimer ; il paraît proche de 3% dans les formes monoostotigues. Une radiothérapie ancienne est retrouvée dans près de la moitié des observations et doit être considérée comme un facteur étiologique ; aussi doit-elle être formellement déconseillée dans cette maladie. L'intervalle moyen entre le diagnostic de dysplasie fibreuse et celui de sarcome atteint 13 ans. La symptomatologie du début de la dégénérescence évoque habituellement une reviviscence de la maladie. C'est encore souligner la nécessité de rebiopsier au moindre doute les lésions évolutives et de pratiquer systématiquement l'ablation de tout foyer de dysplasie fibreuse qui fait parler de lui après la puberté.
TRAITEMENT
Le traitement des formes monoostotiques répond à une triple nécessité affirmer le diagnostic ; éviter les complications mécaniques, traiter les formes évolutives de l'adulte.
1) La biopsie chirurgicale est toujours nécessaire dans ces formes pseudo-tumorales dont elle permet le diagnostic.
2) Le traitement des accidents mécaniques est essentiel. Après la biopsie, la prévention des fractures impose fréquemment un plâtre ou une ostéosynthèse. En cas de fracture, le traitement dépendra de l'âge du blessé, du siège et de la taille des lésions ; le traitement orthopédique est habituellement suffisant chez l'enfant ; l'ostéosynthèse après curetage et greffe est souvent préférable chez l'adulte, surtout si l'ostéolyse est importante.
3) L'ablation du tissu pathologique ne doit pas être systématique dans cette maladie spontanément résolutive. Les lésions de petite taille ou condensées, ou de l'enfant jeune ne nécessitant qu'une simple surveillance jusqu'à la puberté. Les grosses lésions kystiques ou rapidement croissantes justifient par contre un curetage si celui-ci permet d'éviter la fracture. Chez l'adulte la crainte d'une évolution maligne ultérieure autorise une attitude plus interventionniste sur toute lésion symptomatique.
BIBLIOGRAPHIE
l. BALCELLIS C.-A case of polyostotic fibrous dysplasia with sarcomatous change. Méd. Clin. (Barcelone, 1963, 40, 7-11).
2. BELL W.-H.- Fibrosarcomata complicating polyostotic fibrous dysplasia. OraL Surg., 1967,23, 299-310.
3. BETOULIERE P., LAMARCHE, COLIN R. - La forme hypertrophique codensante de la dysplasie fibreuse costale. J. Radio!. Electrol., 1959, 40, 156-157.
4. BROWNBILL D.- A case of malignant transformation in fibrous dysplasia. Aust. New Zeal., J. Surg.,1967, 36, 254-255.
5. BURACZEWSKI J. - Malignant transformation in fibrous dysplasia Pol. Przegl. Radio!., 1969, 33, 541-552.
6. COLE Y B.-L. - Bane sarcoma on polyostotic fibrous dysplasia; Ann. Surg., 1945, 121, 872-881.
7. COSTE F., MASSIASP., MEAUVOISIN F.-Diagnostic entre dysplasie fibreuse ct enchondromatose. A propos d'une observation. Rev. Rhum., 1959, 26, 490-496.
8. DELAHAYE R.-P., LAURENT H., BOURSIQUOT P., JOUFFROY P.-Les aspects radiologiques de la dysplasie fibreuse. J. Radio!. Electrol., 1969, 50, 265-274. 9. DEMARCHI R. - Sulla transformazione sarcomatosa della displasia fibrosa monostotica. Friul. Med.,
1956, 2, 639-649.
10. DE PALMA A.-F., SMYTHE V.-L.-Recurrent fibrous dysplasia in a cortical bane graft. Amer. Orthop. Rel. Res., 1963, 26, 136-144.
11. ELDLING - Dysfibroplasia of bane. Amer. J. Roeng., 1963, 89, 1246-1249.
12. FEINTUCH T.-Chondrosarcoma arising in a cartilaginous aera of fi brous dysplasia. Cancer, 1973,31, 877-881.
13. GIBSON M.-J., MIDDLEMISS J.-H. - Fibrous dysplasia of bane, Brit. J. Radial., 1971, 44, 1-13.
14. GIMES B. - Malignant degeneration of fibrous dysplasia. Fortsch. Roentgenstr., 1970, 113, 211-255.
15. GROSS C.-W. - Fibrous dysplasia and malignant degeneration. Arch. Otol., 1967, 85, 653-657.
16. HARRIS W.-H., DUDLEY R.-H., BARRY R.-1. - The natural history of fibrous dysplasia; an
orthopedie, pathological and roentgenographic study. J. Bane Joint Surg., 1962, 44 A, 207-233.
17. HENRY A. - Monoostotic fibrous dysplasia. J. Bane Joint Surg., 1969, 51 B, 300-306.
18. HOEFFEL H.-C. - Intérêt de la radiologie dans le diagnostic de la dysplasie fibreuse des os. Feuillets d'E.R., 1965, 27.
19. HUVOS A.-G., HIGINBOTHAM, MILLERT R.- Bane sarcoma arising in fibrous dysplasia. Amer. J.Clin. Pathol., 1972, 57, 266.
20. JAFFE H.-L., LICHENSTEIN LN.- Non osteogenic fibroma of bane. Amer. J. Pathol., 1942, 18, 205-221.
21. MAZABRAUD A., SEMAT P., ROZE R.-A propos de l'association de fibromyxome des tissus mous à la dysplasie fibreuse de l'os. Presse Méd., 1967, 18, 665-670.
22.
23. NIWON G.-W., CONDON V.-R. - Epiphyseal involvement in polyostic fibrous dysplasia. Radiology,1973, 106, 167-170.
24. PERKINSON N.-B.-Osteogenic sarcoma arising in polyostotic fi brous dysplasia. Cancer, 1955, 8, 396-402.
25. PICHEN F.-Fibroosteosarcoma of the jaw in a case of polyostotic fi brous dysplasia. Oral. Surg., 1966, 21,778-781.
26. REED R.-J. - Fibrous dysplasia of bane. Arch. Patho., 1966, 75, 480-495.
27. RIDDEL D.-M. - Malignant change in fibrous dysplasia. J. Bane Joint Surg., 1964, 46 B, 251-255.
28. SCHWARTZ D.-T., ALPERT M. -The malignant transformation of fibrous dysplasia. Amer. K. Med.Sei., 1964, 247, 1-20.
29. SETHI R.-J.-Fibrous dysplasia of the rib with sarcomatous charge. J. Bane Joint Surg., 1962, 44 A, 183-188.
30. SLOW 1.-N.- Osteogenic sarcoma arising in a preexisting fibrous dysplasia. J. Oral. Surg., 1971, 29, 126-129.
31. SMITH A.-R. - Malignant change in fibrous dysplasia. Ohio Méd., 1969, 65, 826-829.
32. STEWART M.-J., GLIMER W.-J., EDMONSON A.-J.-Fibrous dysplasia of bane. J. Bane Joint Surg.,1962, 44 B, 302-318.
33. SUTRO C.-J.-Osteogenic sarcoma of the tibia in a limb affected with fibrous dysplasia. Bull. Hosp. Joint.Dis., 1951, 12, 217.
34. TANNER H.-C. - Sarcoma complicating fibrous dysplasia. Oral Surg., 1961, 14, 837-846.
35. VAN HORN P.-E.-Fibrous dysplasia of the femur with sarcomatous change. Amer. J. Ortop., 1963,5,165-167.
36. VAN HORN P.-E., DAHLIN D.-C., BICKEL W.-H.- Fibrous dysplasia. A clinicopathologic study of orthopedie surgical cases. Proc. Maya. Clin., 1963, 38, 175-189.
37. VALLS J., POLAK M., SCHAJOWICZ F.-Fibrous dysplasia of bane. J. Bane Joint Surg., 1950, 32 A,311-322.
38. YANNOPOULOS J.-Osteosarcoma arising on fibrous dysplasia of the facial bones. Amer. J. Surg., 1964, 107, 556-564.
39. ZIMMER J.-F., DAHLIN D.-L., PUGH D.-G., CLAGETI 0.-T.-Fibrous dysplasia of bane analysis of15 cases of surgically verified costal fi brous dysplasia. J. Thorac. Surg., 1956, 31, 488-496.

|
 |
 |
 |
 |
|

